앨나일람, 알츠하이머 RNAi 치료제 기술 공개[이우상의 글로벌워치]
RNA 치료제는 주로 피가 몰려가 표적하기 쉬운 간을 대상으로 개발됐다. 앨나일람은 이번 기술을 적용해 CNS뿐 아니라 눈과 폐에 적용할 수 있는 RNAi 치료제를 개발한다는 계획이다.
8일 업계에 따르면 앨나일람은 세포 내 RNA 발현을 억제하는 짧은간섭 RNA(siRNA)에 친유성(lipophilic) 물질을 결합했다. 이를 CNS와 눈, 폐 등에 전달해 표적 RNA를 억제한 전임상 데이터를 지난 2일 발표했다. 연구 결과는 ‘네이처’의 자매지인 ‘네이처 바이오테크놀로지’ 온라인판 6월호에 실렸다.
앨나일람은 세계 첫 RNAi 치료제인 '온파트로'에 이어 '기블라리', '루마시란' 등 RNAi 신약을 잇달아 출시한 RNAi 치료제 전문 개발기업이다.
앨나일람은 siRNA에 지방산 중 하나인 2’-O-헥사데실(C16)을 결합해 친유성 물질로 만들었다. 물질이 띠는 성질이 친수성이냐 친유성이냐에 따라 세포막을 비롯한 체내 다양한 막을 투과하는 성질이 바뀐다. 케빈 피츠제럴드 앨나일람 최고과학책임자(CSO)는 “siRNA로 CNS와 눈, 폐 관련 질병을 치료할 수 있음을 시사하는 전임상 결과를 얻게돼 기쁘다”고 말했다.
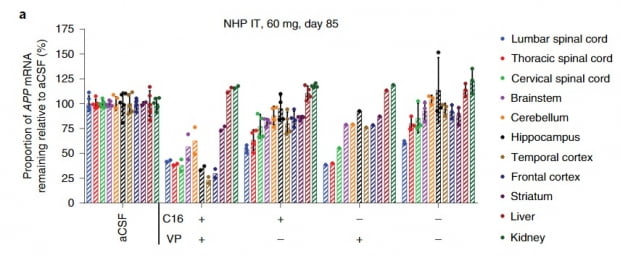
전임상 결과를 보면, 설치류를 이용한 시험에서 C16을 접합한 siRNA는 척수강내(IT) 단일 투여를 통해 뉴런과 성상교세포, 미세아교세포에서 광범위한 흡수가 나타났다. 표적 유전자의 발현을 용량의존적으로 억제했다. 특히 알츠하이머병의 원인으로 꼽히는 아밀로이드베타 단백질의 전구체(APP)를 표적하는 C16-siRNA를 투여한 결과, 척수와 뇌에서 APP가 각각 70%와 80% 감소한 것을 확인했다(최고용량 0.9mg 투여 시). 또 단일 투여만으로도 3개월 동안 효과가 지속됐다. 이는 아두헬름(바이오젠) 및 도나네맙(릴리) 등 항체 위주로 개발이 진행되고 있는 알츠하이머병 치료제에 siRNA가 새로운 대안이 될 수 있음을 시사한다.
또 다른 설치류 실험에서는 C16-siRNA를 비강내 투여를 통해 폐포 및 세기관지에 전달하는 데 성공하기도 했다. 체중 1kg당 10mg 투여로 2개월 동안 표적 유전자인 SOD1 mRNA를 57% 억제했다.
이미 임상은 시작됐다
앨나일람은 신규 플랫폼 기술을 공개하기 앞서 임상 1상에 진입한 상태다. 리제네론과 공동개발 중인 siRNA 기반 알츠하이머병 치료 후보물질 ‘ALN-APP’의 임상 1상(NCT05231785)이 지난 2월부터 시작됐다. 현재 투약이 진행 중이다. 이번 논문에 실린 C16-siRNA 플랫폼 기술이 여기에 쓰였다.환자군(코호트)에 따라 14개월 및 24개월 동안 이상반응(Adverse events)를 보기 위한 임상 1상 연구다. 단회 투여 시 14개월, 다회 투여 시 24개월을 추적 관찰한다. 앨나일람은 임상 1상 연구로 안전성을 최우선적(1차 평가변수)으로 확인하는 것 외에도 뇌척수액에서 알츠하이머병 원인으로 알려진 아밀로이드베타 단백질의 전구체 수준 변화를 관찰할 예정이다. 이 연구를 통해 C16-siRNA 플랫폼의 체내 안전성 및 유효성을 평가한다. 앨나일람은 연말 임상1상 데이터를 확인할 수 있을 것으로 내다봤다.
국내에는 어떤 영향?
국내에서 관련 연구개발을 진행 중인 곳으론 올릭스와 바이오오케스트라가 꼽힌다. 올릭스는 2019년 프랑스 제약사 떼아에 아시아·태평양을 제외한 지역에서의 OLX301 권리를 이전했다. siRNA 신약후보물질 OLX301은 황반변성 치료를 목표하고 있다. 앨나일람과 마찬가지로 유리체 강내 주입술로 영장류에서 전임상 시험을 진행한 결과, 건성 및 습성 노인성 황반변성에서 효력을 확인했다. 올릭스는 올 하반기 OLX301에 대한 임상에 진입한다는 계획이다.바이오오케스트라는 ASO(안티센스올리고뉴클레오티드)를 이용한 알츠하이머병 치료제 후보물질(BMD-001)를 개발하고 있다. ASO는 siRNA와 유사한 기전으로 표적 mRNA와 결합해 단백질 합성을 막는다. 내년 초 미국 식품의약국(FDA)에 임상 1상을 신청할 예정이다. 앨나일람의 ALN-APP가 척수강내 주사로 투여되는 반면, BMD-001은 좀 더 환자 친화적인 정맥주사(IV)를 통한다는 점이 주요 차별점으로 꼽힌다.
이우상 기자 idol@hankyung.com
-
기사 스크랩
-
공유
-
프린트




![월가 "인텔 망가졌다"…구글 9년 만에 최고의 날 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202404/B20240427071917087.jpg)








