신종 코로나의 세포 결합 원천 봉쇄하는 단당류 '표적' 발견
접속 차단 시 바이러스 길어야 5시간 내 소멸
벨기에 루뱅 가톨릭대 연구진, 저널 '네이처 커뮤니케이션' 논문
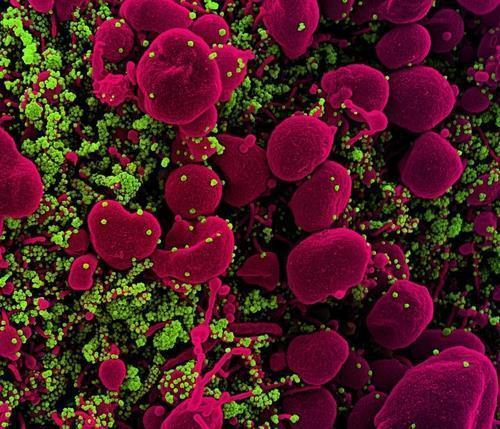
바이러스는 이런 당 잔류물을 보고 침입할 세포를 식별한다.
바이러스가 숙주세포에 달라붙는 표면 '접속점'(point of attachment)은 감염 과정에서 매우 중요한 역할을 한다.
이 접속점은 감염이 시작되는 곳이다.
바이러스가 이를 통해 세포에 들어가야 비로소 감염이 시작된다.
신종 코로나바이러스도 마찬가지다.
세포 표면에서 신종 코로나의 스파이크 단백질(약칭 'S 단백질')이 훨씬 더 강하게 결합하는 이형(異形) 시알산(9-O-acetylated sialic acids)이 발견됐다.
이 시알산은 신종 코로나가 세포의 문을 더 쉽게 열 수 있는 일종의 '열쇠 세트'다.
스파이크 단백질은 바이러스가 세포 내로 쉽게 들어가게 하는 '흡입 컵 효과'(suction cup effect)를 일으킨다.
그래서 신종 코로나가 접속점으로 쓸 수 있는 열쇠(당)를 더 많이 찾을수록 세포 침입로가 더 넓게 열린다.
과학자들은 이형 시알산 등의 접속점을 차단해서 바이러스와 세포의 상호작용을 억제하면 감염을 원천 봉쇄할 수 있다는 것도 확인했다.
벨기에 루뱅 가톨릭대(UCLouvain) 과학자들이 수행한 이 연구 결과는 10일(현지 시각) 저널 '네이처 커뮤니케이션'(Nature Communications)에 논문으로 실렸다.
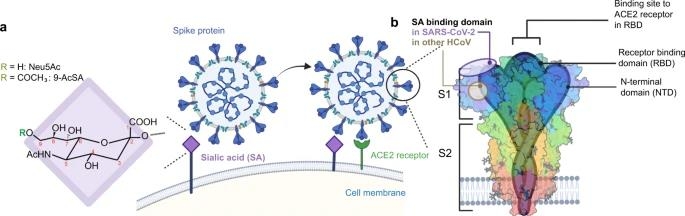
신종 코로나바이러스의 스파이크 단백질이 ACE2와 결합해야 감염 경로가 열리는 것으로 알려졌기 때문이다.
하지만 글리칸(glycan) 같은 세포 접속 인자의 역할에 주목하는 과학자도 적지 않았다.
글리칸은 글리코사이드 결합으로 연결된 다수의 단당류 화합물, 즉 다당류를 말한다.
글리칸은 단당류 잔기의 동종 또는 이종 중합체일 수도 있다.
신종 코로나바이러스는 세포 표면에 도착한 뒤 스파이크 당단백질을 이용해 침입의 교두보를 확보한다.
그런데 여기에도 순서가 있다.
시알산이나 헤파란 황산염(heparan sulfate) 같은 접속 인자에 먼저 달라붙고 그다음에 ACE2 수용체와 결합한다.
스파이크 단백질의 하위 유형인 S1은 ACE2 수용체를 식별하고, S2는 수용체 결합 후 막(膜) 융합을 촉발한다.
글리칸과 결합하는 도메인(GBD)은 S1의 N-말단 도메인(NTD)에 포함돼 있다.
이번에 발견된 변형 시알산은 접속 인자로서 두드러진 역할을 하는 것으로 나타났다.
신종 코로나바이러스는 세포 표면에 착륙한 뒤 다른 당보다 먼저 보통의 친화성을 지닌 변형 시알산과 결합했다.
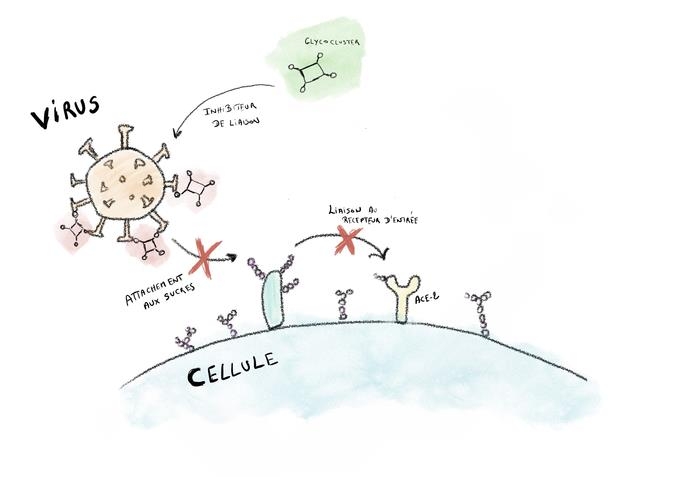
이 차단제는 미리 조절된 수의 시알산 잔기를 전달해 바이러스의 결합 친화성을 높이는 것이다.
예상한 대로 이 차단제는 세포의 정문에 맹꽁이자물쇠를 채우는 것과 비슷한 효과를 냈다.
많은 변형 시알산이 포함된 다원자가(multivalent) 구조(다당류)가 세포 표면에 발현해, 신종 코로나바이러스의 접속 인자 및 수용체 결합과 감염을 모두 차단했다.
세포 결합이 막힌 바이러스는 짧으면 1시간, 길어도 5시간 내로 죽었다.
이 차단제는 신종 코로나의 세포 접촉을 원천 봉쇄한다는 점에서 변이와 상관없이 효과를 볼 거로 기대된다.
루뱅대 연구팀은 조만간 생쥐 모델에 이 차단제를 시험할 예정이다.
이번에 찾아낸 이형 시알산을 기반으로 치료제를 개발하면 여러 가지 편리함도 따를 거로 기대된다.
예컨대 에어로졸(연무제) 형태의 투여가 가능해 환자와의 접촉이나 감염 위험도 피할 수 있다고 한다.
/연합뉴스
-
기사 스크랩
-
공유
-
프린트




![구글, 사상 첫 배당 '주당 20센트'…AI 불안감 덮었다 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202404/B20240426073327760.jpg)








