에이치엘비 "리보세라닙, 1037명 투약환자서 효과 확인"
리보세라닙은 중국에서 위암 3차 치료제로 판매되고 있다. 판매사인 헝루이 및 연구기관들이 리보세라닙을 주제로 12개의 임상결과를 발표했다는 설명이다.
중국에서 시판 이후 138개 병원에서 리보세라닙을 투약받은 환자 1037명의 임상 4상 결과가 나왔다. 총 70%(729명)의 환자에게서 치료효과(DCR)를 확인했고 무진행 생존기간 중간값 (mPFS)은 4.6 개월, 전체 생존기간 중간값(mOS)은 6.57개월이었다. 리보세라닙이 현재 3차 치료제로 시판되고 있어, 2차 치료까지 실패한 환자를 대상으로 진행한 투약 결과임에도 종양 크기가 감소했음을 뜻하는 객관적 반응률(ORR)은 10.7%(111명)로 나타났다.
또 임상환자 1037명 중 평균연령 62세 이상의 고령 환자군 326명에서도 69.8%(228명)의 치료효과(DCR)를 보였다. 무진행 생존기간 중간값은 3.7개월, 전체 생존기간중간값은 7.3개월로 연령에 상관없이 유사한 치료효과를 보였다.
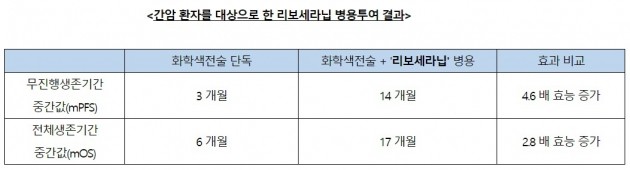
간암 환자를 대상으로 한 리보세라닙과 종양의 크기를 줄이는 화학색전술의 병용요법에서는 기존 임상시험 결과보다 좋은 효능이 입증됐다고 회사 측은 전했다.
간암은 병이 진행된 정도에 따라 치료법이 달라진다. 'Stage C'에 해당하는 간암 환자를 190명까지 확대한 이번 임상시험에서 95명은 화학색전술만, 95명은 리보세라닙과 화학색전술의 병용용법을 비교했다. 화학색전술 단독 치료군의 무진행 생존기간 중간값은는 3개월이었으나, 병용치료군에서는 14개월까지 연장됐다. 전체 생존기간 중간값의 경우 단독 치료군은 6개월이었고, 병용 치료군에서는 17개월로 연장됐다.
에이치엘비의 자회사 LSKB는 현재 리보세라닙의 위암 글로벌 임상 3상을 진행 중이다. 연내 임상을 종료한다는 계획이다.
한민수 기자 hms@hankyung.com
-
기사 스크랩
-
공유
-
프린트





![구글, 사상 첫 배당 '주당 20센트'…AI 불안감 덮었다 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202404/B20240426073327760.jpg)








![죽기 전 17년을 병에 시달려… 건강 검진은 무조건 빨리, 자주 [서평]](https://timg.hankyung.com/t/560x0/photo/202404/01.36534470.3.jpg)