5조 규모 안구건조증 치료제 시장 공략 나선 국내 제약사들
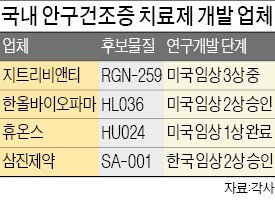
8일 업계에 따르면 안구건조증 치료제 개발에서 속도가 가장 빠른 국내 기업은 지트리비앤티다. 지트리비앤티는 지난 7월 미국 식품의약국(FDA)에서 허가받은 임상 3상의 2차 환자 투여를 최근 완료했다. 내년 FDA 신약 허가를 목표로 하고 있다.
안구건조증은 눈물이 부족하거나 눈물이 많이 증발해 안구 표면이 손상되는 질환이다. 대기 오염, 스마트폰을 비롯한 모바일 기기 확산 등으로 안구건조증 환자는 지속적으로 증가하는 추세다. 시장조사기관 글로벌데이터는 안구건조증 치료제 시장이 2014년 21억5000만달러(약 2조4600억원)에서 2024년 45억9000만달러(약 5조2600억원)로 연평균 7.9% 성장할 것으로 보고 있다.
FDA 허가를 받은 안구건조증 치료제는 두 개에 불과하다. 2003년 승인된 엘러간의 레스타시스와 지난해 허가받은 샤이어의 자이드라가 있다. 자이드라는 지난해 8월 출시돼 4개월여 만에 5400만달러(약 600억원)의 매출을 올렸다.
지트리비앤티는 임상 3상의 2차 투여 결과도 긍정적으로 보고 있다. 이 회사는 3상 1차 투여에서 안구건조증 치료제 후보물질인 RGN-259의 유효성을 확인했다. 2차 투여에서 1차 투여와 같은 결과가 나오면 신약허가 신청 요건을 충족하게 된다. RGN-259는 레스타시스, 자이드라 등 기존 치료제보다 효능이 뛰어나다는 게 회사 측 설명이다. 지트리비앤티 관계자는 “결과가 나오면 기술수출 협상을 본격화할 것”이라고 말했다.
대웅제약과 HL036을 공동 개발 중인 한올바이오파마는 지난달 28일 FDA에서 임상 2상을 승인받았다. 자가면역질환 치료제로 사용되는 항TNF 항체를 안약 형태로 점안 투여하는 바이오베터(바이오의약품 개량신약)다. 한올은 지난달 자가면역질환 항체신약 HL161과 HL036의 중국 사업권을 하버바이오메드에 8100만달러(약 930억원) 규모로 기술수출했다. 내년 8월까지 HL036의 임상 2상을 마칠 계획이다.
휴온스는 연내 FDA에 안구건조증 신약후보물질 HU024의 임상 2상을 신청할 예정이다. 삼진제약은 지난달 식품의약품안전처에서 먹는 안구건조증 치료제로 개발 중인 SA-001의 임상 2상을 승인받았다.
한민수 기자 hms@hankyung.com
-
기사 스크랩
-
공유
-
프린트





![월가 "인텔 망가졌다"…구글 9년 만에 최고의 날 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202404/B20240427071917087.jpg)








