한경 회원에게만 제공되는 특별한 콘텐츠를 만나보세요. 요일별로 다양한 콘텐츠가 제공됩니다.
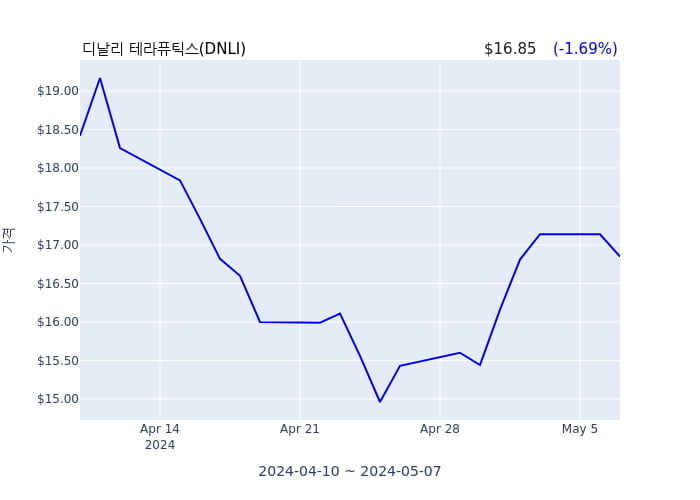
디날리 테라퓨틱스(DNLI) 수시 보고

디날리 테라퓨틱스(DNLI)가 7일(현지 시각) 수시보고서를 제출했다.
[종목 정보 바로가기]
오늘날 경제 발전 속에서 Nasdaq Global Select Market에 거래 기호 DNLI로 상장된 델라웨어 기반 회사인 Denali Therapeutics Inc.는 미국 증권거래위원회에 Form 8-K를 제출했습니다. 보고서는 1934년 증권거래법 제13조 또는 15(d)항에 따라 제출되었습니다.
회사는 2024년 3월 31일에 종료된 회계연도 1분기 재무 결과를 발표하기 위해 2024년 5월 7일에 이 보고서를 발행했습니다. 자세한 보도자료는 보고서에 증거자료 99.1로 첨부되어 있습니다.
161 Oyster Point Blvd., South San Francisco, California에 본사를 둔 Denali Therapeutics는 이 보고서에 제공된 정보가 개정된 1934년 증권거래법 제18조의 목적에 따라 "제출"된 것으로 간주되어서는 안 된다는 점을 추가로 명확히 했습니다. 또한 해당 정보는 해당 서류에 명시적으로 명시되지 않는 한 개정된 1933년 증권법 또는 1934년 증권거래법에 따른 서류에 참조로 포함되지 않을 것이라고 명시했습니다.
Form 8-K는 Denali Therapeutics Inc.를 대신하여 회사의 최고 운영 및 재무 책임자인 Alexander O. Schuth 박사가 서명하고 승인했습니다.
회사의 재무 성과에 대한 자세한 내용은 보도 자료에서 확인할 수 있으며, 이 보도 자료는 Exhibit 99.1에 참조된 문서에서 공개적으로 액세스할 수 있습니다.
Denali Therapeutics는 몇 가지 중요한 사업 하이라이트와 함께 2024년 1분기 재무 결과를 공개했습니다. 혈액뇌관문(BBB)을 통과하도록 설계된 제품 후보를 만드는 데 중점을 두고 있는 캘리포니아에 본사를 둔 바이오제약 회사는 진행 중인 프로젝트에서 긍정적인 발전을 보고했습니다.
주요 하이라이트 중 하나는 WORLDSymposiumTM에서 발표된 MPS II의 tividenofusp alfa에 대한 2년간의 긍정적인 임상 데이터였습니다. 회사는 또한 MPS IIIA 아동을 위한 또 다른 효소 대체 요법인 DNL126에 대한 첫 번째 임상 시험을 시작했습니다.
Denali는 2/3상 HEALEY ALS 플랫폼 시험에서 eIF2B 작용제인 DNL343 프로그램의 등록 단계가 완료되었다고 발표했습니다. 회사는 이번 개발을 신경변성 및 리소좀 축적 질환에 대한 BBB 교차 치료법을 추구하는 데 중요한 이정표로 간주합니다.
지난 2월, Denali는 제20회 연례 WORLDSymposiumTM에서 MPS II의 tividenofusp alfa에 대해 진행 중인 1/2상 연구의 새로운 데이터를 발표했습니다. 데이터는 뇌척수액에서 헤파란 설페이트의 지속적인 정상화, 리소좀 기능 장애 및 신경 손상의 바이오마커의 강력하고 지속적인 감소, 2년간의 치료에 걸쳐 다양한 임상 결과 측정의 개선 및 안정화를 보여주었습니다.
회사는 또한 티비데노푸스 알파(tividenofusp alfa)의 잠재적인 가속화 경로에 관해 FDA의 약물 평가 및 연구 센터와 지속적인 논의를 진행 중이라고 밝혔습니다.
사노피는 다발성 경화증 환자를 대상으로 한 SAR443820/DNL788의 2상 연구에 완전히 등록되었습니다. 그러나 사노피는 2상 HIMALAYA 연구에서 1차 평가변수가 충족되지 않은 후 ALS에 대한 SAR443820/DNL788 개발을 중단했습니다.
마지막으로 Denali는 BIIB122/DNL151의 글로벌 2a상 연구를 위한 협력 및 개발 자금 지원 계약을 발표했습니다. Denali는 파킨슨병 참가자를 대상으로 BIIB122와 관련된 안전성 및 바이오마커를 평가할 계획입니다.
디날리 테라퓨틱스(DNLI)은 7일 전 거래일 종가 대비 1.69% 내린 16.85달러로 장 마감했다.
[해당 공시 바로가기]
<기업소개>
바이오 제약 회사인 Denali Therapeutics Inc.는 미국에서 신경퇴행성 질환의 치료제 후보를 발견하고 개발합니다. 파킨슨병 치료를 위한 1상 및 1b상 임상 시험 중인 소분자 억제제 BIIB122/DNL151을 포함한 류신이 풍부한 반복 키나제 2(LRRK2) 억제제 제품 후보를 제공합니다. 회사는 또한 헌터 증후군 치료를 위한 1/2상 임상 시험 중인 DNL310을 개발합니다. DNL343은 근위축성 측삭 경화증(ALS)의 치료 1상 임상 시험에 있습니다. AR443820/DNL788은 ALS, 다발성 경화증(MS) 및 알츠하이머병 치료를 위한 1상 임상 시험을 완료했습니다. 및 SAR443122/DNL758은 피부 홍반성 루푸스의 치료를 위한 2상 임상 시험에 있습니다. Takeda Pharmaceutical Company, Genentech, Inc., Sanofi, F-star Gamma Limited, F-star Biotechnologische Forschungs-Und Entwicklungsges M.B.H, F-star Biotechnology Limited, SIRION Biotech GmbH, Genzyme Corporation, Harvard University, the Michael J. Fox 재단 및 Centogene; Secarna Pharmaceuticals GmbH & Co. KG와 연구 및 옵션 계약. 퇴행성 신경질환 분야에서 안티센스 치료제 개발 이 회사는 이전에 SPR Pharma Inc.로 알려졌으며 2015년 3월 Denali Therapeutics Inc.로 이름을 변경했습니다. Denali Therapeutics Inc.는 2013년에 설립되었으며 캘리포니아 사우스 샌프란시스코에 본사가 있습니다.
* 이 기사는 한국경제신문과 굿모닝AI리포트가 공동 개발한 인공지능 알고리즘으로 미국 상장사들의 공시를 실시간 분석해 작성한 것입니다. 일부 데이터 수집 과정에서 오류와 지연 등이 있을 수 있으며, 한국경제신문과 콘텐츠 제공 업체는 제공된 정보에 의한 투자 결과에 법적인 책임을 지지 않습니다. 게시된 정보는 무단으로 배포할 수 없습니다.
-
기사 스크랩
-
공유
-
프린트



![서학개미 뒤집어졌다…다우지수 종가기준 첫 4만선 돌파 [뉴욕증시 브리핑]](https://timg.hankyung.com/t/560x0/photo/202405/AD.36579999.1.jpg)





!["한국 가면 꼭 들러야할 곳"…3대 쇼핑성지 '올·무·다' 잭팟 [설리의 트렌드 인사이트]](https://timg.hankyung.com/t/560x0/photo/202405/01.36761565.1.jpg)
