심정지 예측 AI '뷰노메드 딥카스', FDA 혁신의료기기 지정
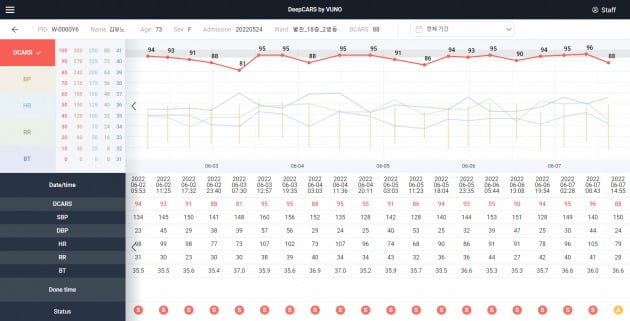
뷰노메드 딥카스는 혈압 맥박 호흡 체온 등 4가지 활력징후를 분석해 환자의 심정지 발생 위험도를 점수로 제공한다. 모든 입원 환자에 대한 상시 감시가 어려운 일반병동에서 의료진의 선제적인 대응을 돕는다.
이 제품은 기존 중증악화 감시(모니터링) 도구 대비 획기적인 기술을 인정받아 FDA로부터 혁신의료기기로 지정됐다고 회사 측은 전했다. FDA의 혁신의료기기(BDD)는 새로운 의료 기술이 시장에 신속하게 진입할 수 있도록 돕는 제도다.
혁신의료기기로 지정되면 FDA 승인 절차에서 우선순위 얻게 된다. 또 승인 과정에서 FDA와 원활한 의사소통을 진행할 수 있다. 이와 함께 유연한 임상연구 설계, 전문 심사팀 배치 등 FDA의 지원을 받을 수 있다.
이번 지정을 통해 뷰노는 미국 진출 준비에 속도를 낼 계획이다. 현재 뷰노는 미국 의료기관과 뷰노메드 딥카스의 임상 연구를 수행하고 있다. 지난달 관련 핵심 기술의 미국 특허를 등록했다.
이예하 뷰노 대표는 “뷰노메드 딥카스는 뷰노의 생체신호 분야 주력 제품으로 이번 FDA 혁신의료기기 지정으로 제품의 혁신성과 우수성을 다시 한번 입증했다”며 “국내에서 도입 병원이 증가하며 시장성을 입증하고 있는 상황에서, FDA 승인을 준비하며 현지 사전 마케팅을 추진하는 등 해외 매출 증대에 매진하겠다”고 말했다.
오현아 기자 5hyun@hankyung.com
-
기사 스크랩
-
공유
-
프린트











![[오늘의 arte] 예술인 QUIZ : 그의 그림 속 인물은 설명되지 않는다](https://timg.hankyung.com/t/560x0/photo/202405/AA.36699526.3.jpg)