천랩 등 마이크로바이옴 업체들, 해외서 속속 신약 임상
고바이오랩도 호주서 임상 시험
지놈앤컴퍼니, 美서 임상 1상 준비
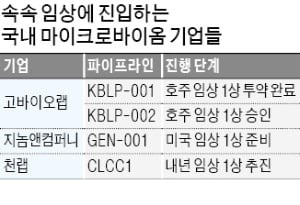
천랩은 지난해 마이크로바이옴 빅데이터를 통해 CLCC1을 발굴하고 전임상에서 고형암에 효과가 있다는 것을 확인했다. 황혜진 천랩 전무는 “호주는 임상시험 승인을 받기가 간편하고 임상시험 비용의 세금을 최대 43.5% 환급받을 수 있는 등 임상하기 좋은 조건을 갖추고 있는 데다 미국과 유럽에 진출하기도 용이하다”며 “내년께 호주에서 임상 1상을 추진할 계획”이라고 말했다.
고바이오랩은 호주에서 임상 1상 시험을 하고 있다. 지난 1월 피험자 36명에게 ‘KBLP-001’ 투약을 마쳤다. 임상에 진입한 국내 최초의 마이크로바이옴 신약 후보물질인 KBLP-001은 아토피, 염증성 장질환, 건선 등 자가면역 질환에 효과가 있을 것으로 회사는 기대하고 있다. 고바이오랩 관계자는 “미국 식품의약국(FDA)에 제출할 임상 2상 시험 계획을 준비하고 있다”고 했다.
지난달에는 ‘KBLP-002’의 호주 임상 1상 승인도 받았다. 이 물질은 아토피성 피부염, 천식 등 알레르기성 면역 질환에 효과가 기대되는 후보물질이다. 올해 임상 1상을 마친 뒤 내년 상반기 미국 임상 2상을 추진할 예정이다.
지놈앤컴퍼니는 마이크로바이옴 기반의 항암제를 개발하고 있다. 신약 후보물질 ‘GEN-001’과 글로벌 제약사 머크와 화이자가 공동 개발한 면역항암제 바벤시오를 병용하는 임상을 추진 중이다. 1월 머크, 화이자와 바벤시오를 임상시험용 의약품으로 무상 공급받는 계약을 체결했다. 회사 측은 100억원 상당의 임상비용을 절감할 수 있을 것으로 추정하고 있다.
전임상에서 GEN-001은 면역관문억제제와 병용했을 때 면역 기능을 활성화하는 데 뛰어난 효과를 보였다. 지놈앤컴퍼니는 FDA에 임상시험계획(IND)을 제출할 준비를 하고 있다. 올 상반기 중 임상 1상에 진입할 예정이다.
임유 기자 freeu@hankyung.com
-
기사 스크랩
-
공유
-
프린트