셀트리온, 아바스틴 시밀러 ‘베그젤마’ 2위 시장 日 허가 획득
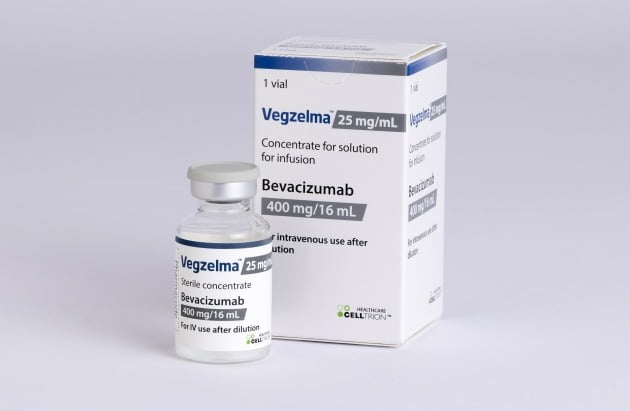
베그젤마가 허가받은 적응증은 전이성 직결장암, 비소세포폐암, 전이성 유방암 등이다.
베그젤마는 지난달 유럽연합집행위원회(EC)에 이어 이달 중순 영국 의약품규제당국(MHRA)의 판매허가도 획득했다. 셀트리온은 지난해 말 식품의약품안전처와 미국 식품의약국(FDA)에도 베그젤마의 판매허가를 신청했다.
셀트리온은 원가 경쟁력을 앞세워 베그젤마를 일본 시장에 조속히 안착시킨다는 방침이다. 회사의 유방암·위암 바이오시밀러 ‘허쥬마’의 일본 내 점유율이 오리지널 의약품보다 높은 것도 긍정적 요인이 될 것으로 봤다.
글로벌 의약품 시장조사기관인 아이큐비아에 따르면 2021년 세계 베바시주맙 시장 규모는 64억3530만달러(약 8조9700억원)다. 이 중 일본이 7억8210만달러(약 1조900억원)를 차지했다. 단일 시장으로 보면 26억200만달러(약 3조6300억)의 미국에 이어 두 번째로 크다.
셀트리온 관계자는 “일본에서 지속 성장 중인 허쥬마에 이어 베그젤마도 조속히 시장에 선보일 것”이라며 “회사의 항암항체 바이오시밀러 제품군(포트폴리오) 강화에 최선을 다하겠다”고 말했다.
이도희 기자 tuxi0123@hankyung.com
-
기사 스크랩
-
공유
-
프린트

![물가 지표 초읽기…다시 파월의 시간이 온다 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202405/B20231109084118397.jpg)