인텔리아 "체내 유전자편집 치료제, 고용량서 9개월 효과 지속"
1회 투여하는 ATTR 치료제
인텔리아와 리제네론은 트랜스티레틴 아밀로이드증(ATTR) 치료제로 개발 중인 NTLA-2001의 갱신된 임상 1상 1단계 중간 결과를 유럽간학회(EASL 2022)에서 공개했다고 지난 24일(현지시간) 밝혔다.
ATTR은 ‘TTR’ 유전자에 돌연변이를 가지고 태어난 사람에서 발생하는 유전성 질환이다. 간에서 비정상적인 TTR 단백질이 생겨 단백질응집체인 아밀로이드로 쌓인다. 그 결과 심장, 신경계, 소화계 등 여러 조직에서 합병증이 나타난다.
인텔리아와 리제네론은 크리스퍼 캐스나인(CRISPR Cas9) 유전자편집 기술을 적용한 NTLA-2001을 ATTR 치료제로 개발하고 있다. 인체 내에서 유전자를 편집해 TTR 단백질 감소를 유도하는 기전이다. 1회 투여로 영구적인 치료를 목표한다.
임상 1상은 다발신경병증이 있는 유전성 ATTR(ATTRv-PN) 및 심근병증을 동반한 ATTR(ATTR-CM)을 대상으로 진행 중이다.
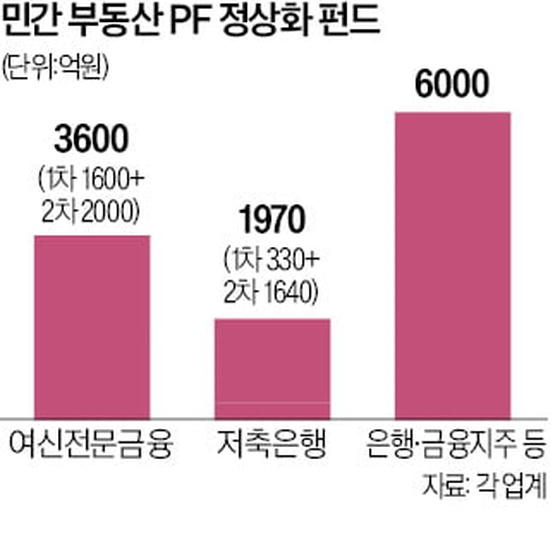
인텔리아는 임상 1상 중 ATTRv-PN 환자 15명을 대상으로 진행된 4개 용량 환자군의 추적 결과를 발표했다. 혈청 내 TTR 단백질의 감소(Serum TTR reductions) 상태가 지속되는 것을 확인했다.
최고 용량인 체중 1kg당 1mg를 투여받은 환자군 6명은 투여 후 28일을 기준으로 TTR이 평균 93% 및 최대 98% 줄었다. 1mg 투여군은 TTR의 감소 상태는 평균 6개월 동안 유지되고 있다. 3명의 환자는 TTR 감소 상태가 9개월째에 들어섰다.
0.7mg 투여군은 28일째에 관찰된 86%의 TTR 감소가 6개월 동안 지속되고 있다. 0.1mg 및 0.3mg을 투여받은 환자들은 추적관찰 기간이 12개월에 들어섰다. 치료 반응은 지속되고 있다. 특히 0.3mg 투여군은 89%의 TTR 감소를 유지 중이다.
임상 1상 2단계로 80mg 고정용량 투여
4가지 용량의 환자군은 중앙값이 10개월인 추적기간 동안 우수한 내약성이 관찰됐다. 환자의 73%가 중증도 최대 1등급의 이상반응을 보고했다. 1mg 투여군의 가장 빈번한 이상 반응은 두통, 주입 관련 반응, 요통, 발진 및 메스꺼움 등이었다.인텔리아는 임상 1상의 두 번째 단계에서 고정용량으로 80mg 투여를 진행 중이다. 체중과 관계 없이 80mg을 투여하는 것이다. 임상 1상 1단계 진행 상황 및 약동학 가상시험(시뮬레이션) 등을 근거로 체중 1kg당 1mg 투여 결과와 유사한 효과가 나타날 것으로 예상 중이다.
존 레너드 인텔리아 대표는 “안전성과 내구성을 확인하는 결과를 공유하게 돼 기쁘다”며 “일회 투여로 전신에 전달되고 장기간 지속되는 크리스퍼 기반 치료제에 대한 확신을 높였다”고 말했다.
ATTR-CM 환자군에 대한 임상 1상 첫 번째 중간 결과는 올 하반기에 발표할 예정이다.
박인혁 기자 hyuk@hankyung.com
-
기사 스크랩
-
공유
-
프린트


![월가 '대장 개미' 트윗 한 줄에…밈 주식 동반 폭등 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202405/B20240514073731743.jpg)