발암물질 포함 고혈압약 리스트 115개는?
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트

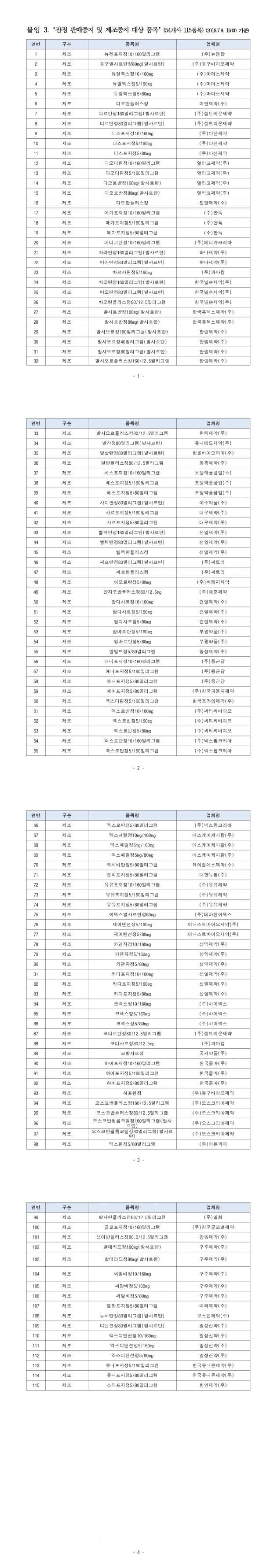
10일 식품의약품안전처(이하 식약처) 홈페이지, 페이스북, 블로그에는 중국 제지앙 화하이사(社)가 제조한 원료의약품 발사르탄(Valsartan)이 사용될 가능성이 있는 제품 리스트가 게재됐다.
식약처는 고혈압 치료제 219개 품목(82개 업체) 전체를 지난 7월7일부터 점검한 결과 해당 원료를 사용하지 않은 것으로 확인된 104개 품목(46개 업체)은 판매중지 및 제조중지를 해제했다.
하지만 해당 원료 사용이 확인된 115개 품목(54개 업체)은 판매중지 및 제조중지를 유지하고 회수를 진행한다. 이 중 18개 업체의 경우 해당 원료를 사용한 품목과 사용하지 않은 품목이 있었다.
식약처는 이번 조치 대상 제품을 복용 중인 환자는 해당 의약품을 처방받은 병,의원 등 의료기간에 상담을 거쳐 처방을 변경 받을 것을 당부했다.
해당 원료를 사용한 제품을 처방받았는지에 대한 사항은 진료 의료기관이나 약국에서 확인할 수 있다.
<잠정 판매중지 및 제조중지 대상 품목>

NDMA는 WHO 국제 암연구소(IARC) 2A, 즉 인간에게 발암물질로 작용할 가능성 있는 물질로 분류됐기 때문이다.
식약처는 이번 문제가 된 ‘발사르탄’이 함유된 모든 의약품의 경우 의사 처방에 따라 약국에서 조제 후 복용할 수 있는 전문의약품으 로서 ‘의약품 안전사용서비스(DUR)’ 시스템에 ‘처방 금지’ 경고 문구가 등록되어 의사가 처방할 수 없어 환자들이 사용하거나 유통 되는 것이 원천 차단된다고 밝혔다.
한경닷컴 뉴스룸 newsinfo@hankyung.com
ADVERTISEMENT
ADVERTISEMENT





![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


