美 FDA, 코로나19 치료제로 ‘렘데시비르’ 정식 사용 승인
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
첫 FDA 승인 코로나19 치료제
지난 5월 긴급사용 승인 후 정식 허가
지난 5월 긴급사용 승인 후 정식 허가

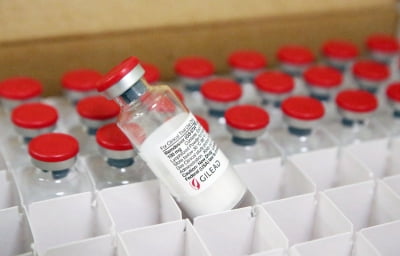
이번 허가로 렘데시비르는 미국에서 코로나19 치료용으로 승인받은 첫 의약품이 됐다.
22일(현지시간) 외신 보도에 따르면 미 식품의약국(FDA)은 항바이러스제인 렘데시비르를 코로나19 입원 환자 치료에 쓸 수 있다고 정식 허가했다. 지난 5월 FDA로부터 긴급 사용 승인(EUA)을 받은 지 5개월 만이다.
멀대드 퍼시 길리어드사이언스 수석의학책임자는 공개서한에서 “렘데시비르는 코로나19로 입원 치료를 받는 환자가 더 빨리 회복하게 돕는 것으로 증명된 첫 항바이러스 약물”이라고 설명했다.
이어 “내부 제조 역량을 늘리고 외부 제조망을 확대해 다음 주에 세계적으로 적절한 환자 치료에 약물이 충분히 공급될 수 있게 할 것”이라고 덧붙였다.
회사 측은 이달 말까지 렘데시비르 생산량이 글로벌 수요를 맞출 수 있을 것으로 기대하고 있다. 앞서 길리어드는 연말까지 200만명 투여분 이상을 생산하고, 내년에 수백만회분을 추가로 더 만들 계획이라고 밝혔다.
대니얼 오데이 길리어드 최고경영자(CEO)는 “코로나19 대유행 시작부터 길리어드는 글로벌 보건 위기의 해법을 찾는 데 도움을 주기 위해 끊임없이 노력했다”며 “1년도 안 돼 미국에서 이 약을 필요로 하는 모든 환자에게 사용 가능하다는 FDA 승인을 얻게 된 것이 믿기지 않는다”고 말했다.
렘데시비르는 원래 에볼라 치료제로 개발된 정맥주사 형태의 약이다. 코로나19에 감염된 도널드 트럼프 미국 대통령에게 투여된 치료제 중 하나이기도 하다.
김예나 기자 yena@hankyung.com
ADVERTISEMENT
ADVERTISEMENT



![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


