변방에서 중원으로…글로벌 투자 행사 나란히 선 'K바이오 투톱'
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
JP모간 헬스케어 콘퍼런스
김태한 삼바 사장, 올해 제3공장 수주율 50%로
"모든 회계처리 국제기준 맞춰 적법하게 해왔다"
서정진 셀트리온 회장, 中서도 바이오시밀러 개발
"내년 최대 5조원 공급 능력 갖추도록 준비할 것"
김태한 삼바 사장, 올해 제3공장 수주율 50%로
"모든 회계처리 국제기준 맞춰 적법하게 해왔다"
서정진 셀트리온 회장, 中서도 바이오시밀러 개발
"내년 최대 5조원 공급 능력 갖추도록 준비할 것"

김태한 삼성바이오로직스 사장은 국내 기업 중 처음으로 가장 큰 행사장인 그랜드볼룸에서 발표했다. 800석 규모의 그랜드볼룸을 지정받은 곳은 노바티스, 존슨앤드존슨 등 글로벌 기업들이다. 그랜드볼룸에서 발표한 아시아 기업은 삼성바이오로직스와 일본 다케다뿐이다.
서정진 셀트리온 회장도 바로 옆 500석 규모 콜로니얼룸에서 발표해 투자자들의 관심을 받았다. 지난해에는 이머징마켓(신흥시장) 부문으로 분류돼 50석 규모의 작은 방을 썼지만 올해 글로벌 플레이어로 올라선 셈이다.
대규모 수주 나서는 삼성 바이오로직스
김태한 삼성바이오로직스 사장(왼쪽)은 “생산 수준의 25%까지 확보한 인천 송도 3공장의 수주 규모를 연내 50%로 확대하겠다”고 밝혔다.
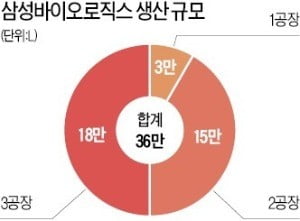
삼성바이오로직스는 2017년 세포주 개발, 임상물질 생산, 품질 테스트 등의 서비스를 제공하는 CDO·CRO 사업에 진출했다. CMO 이전 과정까지 사업 영역을 확대한 것이다. 김 사장은 “이달 기준으로 CMO 27건, CDO·CRO 41건을 각각 수주했다”고 밝혔다.
삼성바이오로직스는 지난해 10월부터 한 번에 18만L를 생산할 수 있는 세계 최대 규모의 3공장을 가동했다. 3공장 생산 규모의 25%까지 수주를 확보한 데 이어 연내 수주 물량을 50%로 끌어올린다는 계획이다. 김 사장은 “단일항체 바이오의약품 시장은 지난해 이후 연간 약 12%씩 성장할 것”으로 전망했다.
삼성바이오로직스가 CMO 비즈니스의 패러다임을 바꿨다는 점도 강조했다. 경쟁사보다 공장 건설과 가동에 필요한 기간을 40% 가까이 단축하고 설립 7년 만에 세계 최대 규모의 CMO 기업으로 올라섰기 때문이다.
김 사장은 4공장 증설 계획에 대해 “우선 3공장 가동률을 매년 20%씩 점진적으로 높여 2020년이면 완전 가동될 것”이라며 “바이오젠이 개발 중인 알츠하이머 치료제 아두카누맙의 성공 여부가 결정되는 2020년 증설을 고려할 수 있다”고 말했다. 이어 “알츠하이머 치료제가 성공한다면 수요가 폭발적이기 때문에 4공장뿐만 아니라 5, 6공장도 지을 수 있다”고 덧붙였다.
김 사장은 분식회계 문제에 대해서도 자세히 설명했다. 김 사장은 발표 시작부터 회계 이슈를 비중있게 다뤘다. 모든 회계 처리를 IFRS에 맞춰 적법하게 해왔고 다수의 글로벌 회계법인과 한국공인회계사회 등을 통해서도 회계 처리의 적법성을 인정받았다는 점도 강조했다.
셀트리온 상반기 중국에 합작 법인
“2020년 최대 45억달러(약 5조원)의 공급 능력을 갖출 수 있게 준비하고 있습니다.”
서정진 셀트리온 회장(오른쪽)의 말이다. 그는 “바이오시밀러(바이오의약품 복제약) 분야에서 자체 기술력을 바탕으로 성장한 셀트리온그룹이 글로벌 바이오·제약기업으로의 도약을 눈앞에 두고 있다”며 이렇게 밝혔다.
올해부터 항체 바이오시밀러 램시마SC가 출시되고 트룩시마, 허쥬마가 유럽과 미국을 비롯한 세계에서 판매되기 때문이다. 서 회장은 “지난해 유럽 허가를 신청한 램시마SC가 도약의 구심점이 될 것”이라며 “램시마SC 허가 후 유럽을 시작으로 글로벌 직판 시스템을 완성해 셀트리온그룹을 글로벌 바이오·제약기업으로 키우겠다”고 강조했다.
셀트리온그룹은 올해 유럽에서 램시마SC의 허가를 기다리고 있다. 유럽에서 약 56%의 시장 점유율을 달성한 램시마IV에 이어 시장 판도를 바꿀 ‘게임 체인저(Game Changer)’가 될 것으로 회사 측은 기대하고 있다.
서 회장은 세계 2위 규모 제약시장인 중국에서 바이오 및 케미컬의약품 사업을 본격적으로 추진하겠다고도 했다. 그는 “올 상반기 중국 합작법인 설립을 완료할 계획”이라며 “중국으로 기술을 이전하고 현지에 공장을 지어 중국 판매 제품은 중국에서 생산할 것”이라고 말했다.
셀트리온은 2017년 5월 중국식품약품감독관리국(CFDA)으로부터 램시마 임상시험을 승인받아 임상을 진행 중이다. 중국에서 해외 기업 바이오시밀러가 임상 승인을 획득한 첫 사례다.
서 회장은 합성의약품 사업 진출 중요성도 강조했다. 그는 “합성의약품 시장은 약 1000조원 규모로 세계 제약시장 매출의 3분의 2를 차지한다”며 “케미컬의약품 생산을 위해 2015년 셀트리온제약 청주공장을 준공했으며 에이즈 치료제를 중심으로 시장성 있는 케미컬의약품 포트폴리오를 완성해 왔다”고 설명했다.
서 회장은 “셀트리온제약 청주공장의 미국 식품의약국(FDA) 우수화장품 제조 및 품질관리기준(cGMP) 승인 획득과 유럽 규제기관(MHRA) 실사 완료로 글로벌 케미컬의약품 공급 준비를 완료했다”며 “지난해 첫 케미컬의약품인 에이즈 치료제 ‘테믹시스’도 FDA로부터 허가받았고 국제조달 시장 공급자로도 선정됐다”고 말했다.
샌프란시스코=전예진 기자 ace@hankyung.com
ADVERTISEMENT
ADVERTISEMENT




![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


