대웅제약, '나보타' 공장 FDA 실사 완료…소송 상관 없이 美 수출 추진
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
향남 나보타 제2공장 최근 FDA 실사 완료
내년 FDA 승인 후 국내 세번째 cGMP 공장 목표
메디톡스가 제기한 균주 소송 내년 상반기 본격화
나보타 균주 출처와 유전자 염기서열 공방 예상
내년 FDA 승인 후 국내 세번째 cGMP 공장 목표
메디톡스가 제기한 균주 소송 내년 상반기 본격화
나보타 균주 출처와 유전자 염기서열 공방 예상

◆ FDA 실사 통과 기대감
ADVERTISEMENT
그러나 이곳에서 만든 제품을 미국으로 수출하려면 약 2년 간 FDA의 까다로운 심사를 거쳐야한다. FDA의 허가를 받으면 해당 공장은 선진우수의약품 제조 및 품질관리기준(cGMP)을 갖춘 것으로 평가된다. 공장 설비가 다 지어졌더라도 cGMP 통과 전에는 ‘기계적 완공’이라 부르는 것은 이런 이유에서다.
우리나라에서 cGMP 인증을 받은 회사는 바이오시밀러를 생산하는 셀트리온과 삼성바이오로직스 두 곳 뿐이다. 완성된 의약품 품질 뿐만 아니라 생산 공정과 설비, 관리 기준을 엄격하게 평가하기 때문에 수년동안 cGMP 인정을 받지 못하는 사례가 많다. 대웅제약은 항생제 제네릭 ‘메로페넴’의 미국 허가를 받은 경험이 있어 이번 나보타 공장도 실사를 통과할 수 있을 것으로 기대하고 있다.
ADVERTISEMENT
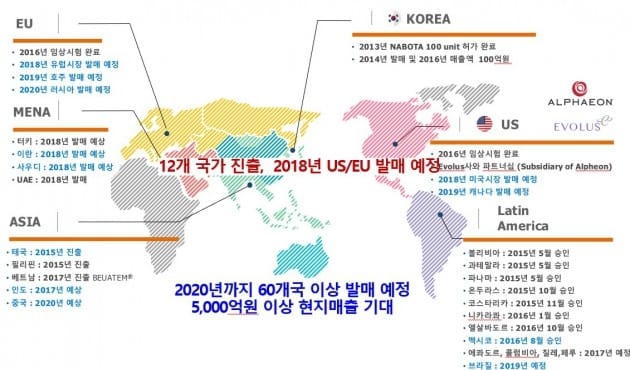
사전 계약을 통해 해외 수출 물량도 확보했다. 나보타는 내년 미국, 유럽 뿐만 아니라 중동, 터키, 인도네시아에 발매하고 2019년 캐나다, 호주, 브라질, 홍콩에 진출할 계획이다. 대웅제약은 나보타 매출이 올해 200억에서 내년 600억원, 수출이 본격화되는 2019년에는 1200억원으로 늘어날 것으로 보고 있다.
◆내년 균주 도용 소송 본격화
ADVERTISEMENT
대웅제약은 나보타 균주 발견과 신고 절차가 적법하게 이뤄졌다며 메디톡스의 주장을 전면 부인했다. 자연상태에서도 균주 발견이 가능하고 균주의 염기서열은 보툴리눔 톡신의 안전성, 유효성과 관계가 없기 때문에 중요하지 않다는 입장이다.
박 본부장은 “보툴리눔 톡신은 제조기술이 핵심으로 특허 받은 제조방법으로 고도화된 품질 수준을 보유한 대웅제약이 메디톡스의 공정을 도용할 이유가 없다”며 “나보타 미국 진출을 지연시키려는 의도”라고 말했다.
ADVERTISEMENT
업계는 양측이 첨예하게 대립하고 있는데다 균주와 관련한 민사소송 전례가 없는 만큼 소송에 시간이 걸릴 것으로 내다보고 있다. 제약업계 관계자는 “한국 소송 결과가 미국 소송에도 영향을 미치기 때문에 예의주시할 수밖에 없다”며 “양측의 진흙탕 싸움이 계속되면 한국 보툴리눔 톡신 제제에 대한 대외 신뢰도 하락도 불가피할 것”이라고 말했다.
전예진 기자 ace@hankyung.com
ADVERTISEMENT
ADVERTISEMENT