지놈앤컴퍼니 자회사, 뇌질환 치료제 美 임상 1상 승인
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
사이오토 바이오사이언스
오는 7월 첫 투약 예정
오는 7월 첫 투약 예정
지놈앤컴퍼니는 자회사 사이오토 바이오사이언스(Scioto Biosciences)가 미국 식품의약국(FDA)으로부터 뇌질환 마이크로바이옴 치료제 ‘SB-121’의 임상 1상을 승인받았다고 31일 밝혔다.
사이오토 바이오사이언스는 오는 7월부터 미국 신시네티 어린이병원(Cincinnati Children’s Hospital Medical Center)에서 자폐증(ASD) 환자를 대상으로 첫 투약을 진행할 예정이다. 임상은 위약 대조, 이중맹검 방식으로 4주간의 투약기간을 포함해 총 17주 간 진행된다.
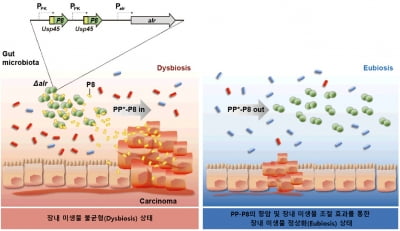
SB-121은 사이오토 바이오사이언스가 ASD를 주요 적응증으로 개발 중인 마이크로바이옴 치료제다. 산모의 모유 안에 있는 락토바실러스 루테리 균주에 사이오토 바이오사이언스 'ABT' 플랫폼 기술을 적용해, 균주의 체내 안정성과 효능을 높였다는 설명이다.
전임상에서 체내 옥시토신 분비를 장시간 유지시키는 것을 확인했다. 옥시토신은 자폐증 완화에 영향을 미치는 것으로 알려져 있다.
회사는 임상 1상에서 SB-121의 반복투여를 통한 안전성과 초기 유효성을 평가할 예정이다. 작년 11월에는 건강인 대상 신생아괴사성장염(NEC)을 적응증으로 FDA의 임상 1상을 승인받았다. 사이오토 바이오사이언스는 내년 ASD 임상 2상 및 NEC 임상 1·2상을 진행할 계획이다.
배지수 지놈앤컴퍼니 대표는 “‘장-뇌-축(gut-brain-axis)’ 이론을 바탕으로 한 마이크로바이옴 뇌·신경 질환 치료제 개발 영역은 마이크로바이옴 산업에서 빼놓을 수 없는 중요한 분야”라며 “이번 임상에서 유의미한 결과를 도출해 최초의 마이크로바이옴 뇌·신경 질환 치료제 개발 가능성을 높일 것”이라고 말했다.
김예나 기자
사이오토 바이오사이언스는 오는 7월부터 미국 신시네티 어린이병원(Cincinnati Children’s Hospital Medical Center)에서 자폐증(ASD) 환자를 대상으로 첫 투약을 진행할 예정이다. 임상은 위약 대조, 이중맹검 방식으로 4주간의 투약기간을 포함해 총 17주 간 진행된다.
SB-121은 사이오토 바이오사이언스가 ASD를 주요 적응증으로 개발 중인 마이크로바이옴 치료제다. 산모의 모유 안에 있는 락토바실러스 루테리 균주에 사이오토 바이오사이언스 'ABT' 플랫폼 기술을 적용해, 균주의 체내 안정성과 효능을 높였다는 설명이다.
전임상에서 체내 옥시토신 분비를 장시간 유지시키는 것을 확인했다. 옥시토신은 자폐증 완화에 영향을 미치는 것으로 알려져 있다.
회사는 임상 1상에서 SB-121의 반복투여를 통한 안전성과 초기 유효성을 평가할 예정이다. 작년 11월에는 건강인 대상 신생아괴사성장염(NEC)을 적응증으로 FDA의 임상 1상을 승인받았다. 사이오토 바이오사이언스는 내년 ASD 임상 2상 및 NEC 임상 1·2상을 진행할 계획이다.
배지수 지놈앤컴퍼니 대표는 “‘장-뇌-축(gut-brain-axis)’ 이론을 바탕으로 한 마이크로바이옴 뇌·신경 질환 치료제 개발 영역은 마이크로바이옴 산업에서 빼놓을 수 없는 중요한 분야”라며 “이번 임상에서 유의미한 결과를 도출해 최초의 마이크로바이옴 뇌·신경 질환 치료제 개발 가능성을 높일 것”이라고 말했다.
김예나 기자

![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


