카이노스메드, 파킨슨병 치료제 미국 FDA 임상 2상 '승인'
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
지난달 식품의약품안전처에서 다계통위축증(MSA) 2상을 승인받은 데 이은 것으로, KM-819의 임상 개발이 국내외에서 본격화됐다는 설명이다.
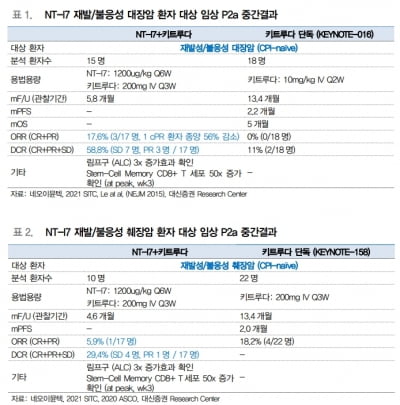
카이노스메드는 임상기관들과 계약 이후 환자 모집에 나서게 된다. 2상은 크게 두 부분으로 나눠 진행할 계획이다. 건강하고 나이 많은 참가자 18명과 파킨슨병 환자 24명을 대상으로 KM-819를 200mg 400mg 800mg씩 투여해 적정 용량을 확정할 예정이다. 1상에서는 부작용 없이 400mg까지 투여했다.
용량이 결정되면 미국 내 병원에서 환자 288명을 대상으로 2년간 임상을 진행하게 된다. 특정 유전자(GBA) 변이가 있는 환자의 줄기세포를 이용한 실험에서 효능을 확인함에 따라 이 임상에 유전자 변이 환자를 포함하기로 했다.
KM-819는 세포의 죽음을 촉진하는 'FAF1' 단백질의 과발현을 억제해 신경세포의 사멸을 막는다. 또 자가포식(autophagy) 기능을 활성화해 알파시누클라인의 축적을 억제한다. 2상에서 효능을 보이면 최초의 질환조절 효능이 있는 약물이 된다고 회사 측은 강조했다.
카이노스메드는 2상에서 효능을 확인한 후 글로벌 제약사로 기술이전을 추진할 계획이다. 파킨슨병은 현재 증상완화제만 있으며 근본적인 질병조절 치료제가 없는 상황이다.
한민수 기자
-
기사 스크랩
-
공유
-
프린트



![고용보고서 앞두고 혼조 마감…엔비디아, 시총 3위로 밀려 [뉴욕증시 브리핑]](https://timg.hankyung.com/t/560x0/photo/202406/01.34384444.1.jpg)






![[공연소식] 국립극단 창작 연극 '전기 없는 마을' 내달 초연](https://timg.hankyung.com/t/560x0/photo/202406/ZK.36961180.3.jpg)