보령바이오파마, A형간염 백신 출시
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
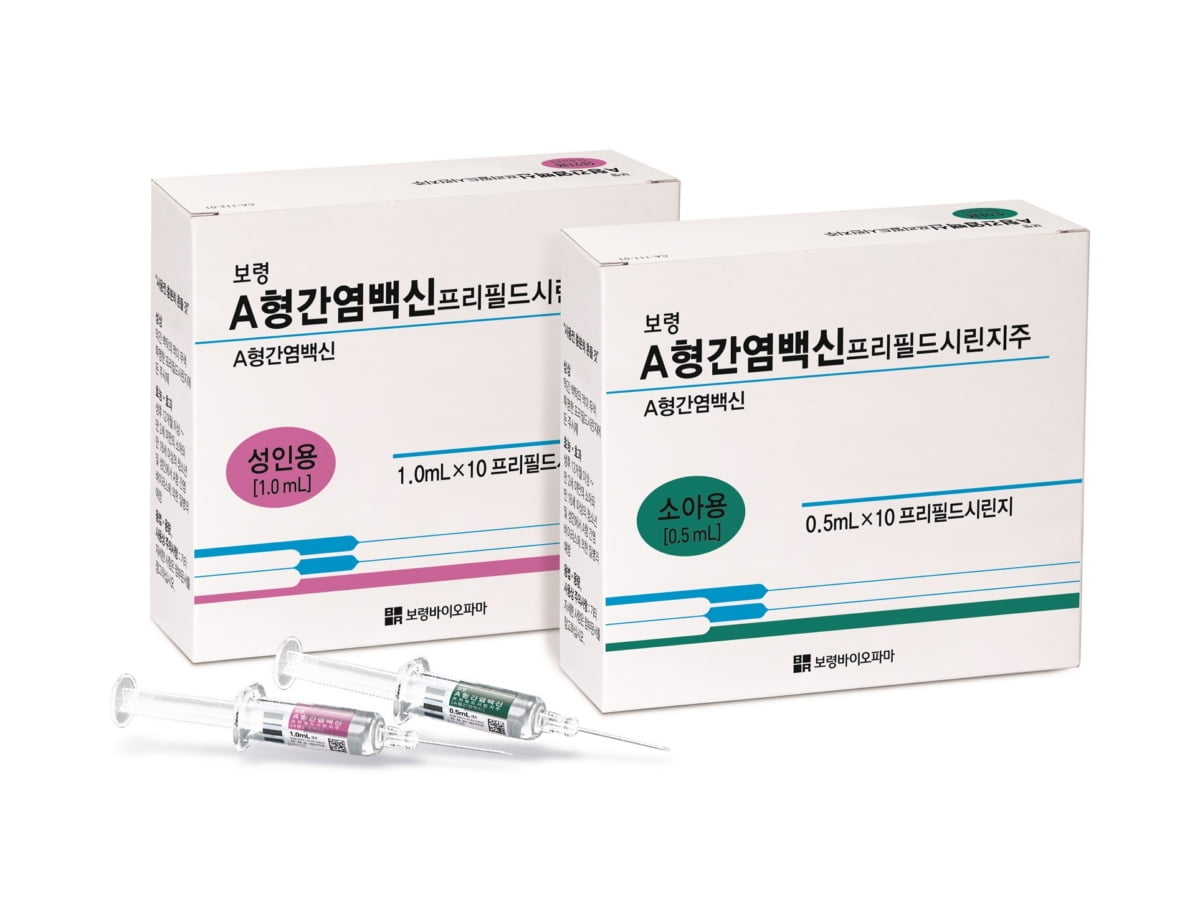
A형간염 백신은 지난 2015년 국가예방접종(NIP)으로 전환됐지만 수입 완제품 3종만 공급돼 왔으며, 국내 제품은 없었다.
이에 따라 매년 국내 상황에 맞는 충분한 공급이 이뤄지지 않아 의료 현장의 수급 불안정이 지속됐다.
보령바이오파마는 이러한 수급 불안정을 해소하기 위해 지난 2012년 세포배양 방식의 A형간염 백신 개발에 착수, 지난해 12월 식약처로부터 품목허가를 받았다.
임상시험은 2017년부터 만 12~23개월, 만16세 이상으로 나눠 각각 24개월, 16개월간 진행했으며, 6~12개월 간격의 총 2회 접종에서 대조군 대비 면역원성의 비열등성과 안전성을 입증했다.
특히 소아 대상 임상시험에서는 2차 접종 후 1개월째 시험군의 항체가는 대조군 대비 약 3.5배 이상 높아 매우 우수한 면역원성을 형성했음을 확인했다.
A형간염은 국내에서는 20~40대 연령층에서 많이 발생하고 있고, 감염되면 고열, 구토, 황달 등의 증상이 나타난다.
장홍두 보령바이오파마 마케팅본부 상무는 "한국인을 대상으로 임상을 진행하고 진천 공장을 통해 국내 제조하는 최초의 A형간염 백신이라는데 의의가 있다"며 "백신 수급 안정과 질병 예방에 기여하겠다"고 말했다.
문형민기자 mhm94@wowtv.co.kr
ⓒ 한국경제TV, 무단 전재 및 재배포 금지
![[포토] 한경 창간 60주년 독자이벤트 성황리에 마무리](https://img.hankyung.com/photo/202411/01.38726908.3.jpg)


![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


