코오롱티슈진, 인보사 美 임상 3상 본격 돌입
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
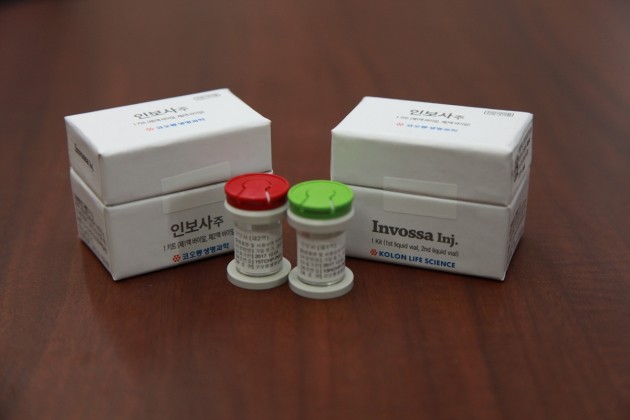
코오롱티슈진은 미국 식품의약국(FDA)로부터 임상시료 사용허가를 받았다고 6일 밝혔다. FDA는 2015년 5월 코오롱티슈진에 인보사의 임상 3상을 허가했다. 코오롱티슈진은 그동안 임상 3상에 사용할 임상용 의약품 허가를 위한 공정을 진행해왔다. 이번 허가로 임상 3상을 본격적으로 시작할 수 있게 됐다.
인보사의 미국 임상 3상은 약 1020명의 환자를 대상으로 50여개 임상기관에서 진행될 예정이다. 코오롱티슈진은 임상병원과의 계약 및 각 병원의 임상시험심사위원회와의 협의가 마무리되는 올 3분기께 환자 등록과 투여를 시작할 수 있을 것으로 보고 있다
인보사는 지난해 7월 식품의약품안전처로부터 신약 허가를 받아 같은해 11월부터 국내에서 판매 중이다. 7개월 만에 처방건수 1000건을 돌파하는 등 시장에 안착하고 있다는 설명이다. 홍콩과 마카오, 몽골, 아랍에미리트공화국, 사우디아라비아 등으로의 수출계약도 체결한 상태다.
이번 미국 임상 3상에는 통증 완화와 기능성개선 효능은 물론 골관절염의 근본 치료제 지정을 위한 시험계획도 포함돼 있다. FDA로부터 골관절염의 근본 치료제로 지정되면 세계 최초다.
한민수 기자 hms@hankyung.com
ADVERTISEMENT
ADVERTISEMENT




![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


