점유율 50% 돌파 가능성 커져
'퍼스트 무버' 효과로 시장선점
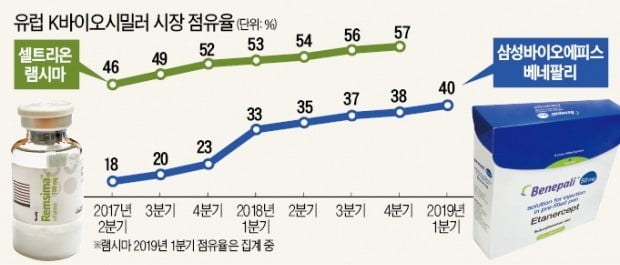
제약·바이오업계는 램시마에 이어 연내 오리지널 바이오의약품을 넘어서는 K바이오시밀러가 탄생할 것으로 내다보고 있다. 가능성이 높은 것은 삼성바이오에피스가 2016년 1월 유럽에 처음 출시한 ‘베네팔리’다. 시장조사업체 아이큐비아에 따르면 베네팔리는 출시 3년째인 올 1분기 40%의 점유율을 기록했다. 2017년 10%대에 불과했던 시장 점유율은 지난해 1분기 30%대에 진입했고 올해 처음 40%대에 올라섰다. 연내 50%를 돌파하고 오리지널 제품인 화이자의 ‘엔브렐’을 추월할 것이라는 전망이 나온다.
셀트리온 트룩시마도 급속도로 처방이 확대되고 있다. 2017년 2분기 유럽에 출시된 트룩시마는 그해 4분기 18%의 점유율을 기록했고 작년 4분기에는 전년의 두 배인 36%로 점유율이 급등했다. 올 연말 50%를 돌파할 가능성도 제기된다. 이렇게 되면 오리지널을 넘어선 K바이오시밀러는 3개로 늘어나게 된다.
업계는 국산 바이오시밀러가 퍼스트무버(시장 개척자)의 이점을 살려 시장 선점에 성공한 것으로 분석하고 있다. 이들 제품은 시장에 가장 먼저 출시된 퍼스트무버라는 공통점이 있다.
램시마는 존슨앤드존슨의 레미케이드를 복제한 바이오의약품으로 세계 최초의 바이오시밀러라는 기록을 보유하고 있다. 베네팔리와 트룩시마는 각각 화이자의 엔브렐, 로슈의 리툭산을 복제한 제품으로 유럽에서 처음 허가를 받은 바이오시밀러다.
퍼스트무버는 경쟁 제품보다 시장에 먼저 침투할 수 있고 처방이 늘수록 환자 데이터를 더 많이 축적할 수 있다. 후발 제품이 나오더라도 의료진이 안전성과 효능이 입증된 의약품을 선호하기 때문에 가격 경쟁력이 없다면 시장의 판도를 바꾸기가 쉽지 않다.
국산 바이오시밀러에 대한 우호적 인식이 형성됐다는 점도 영향을 미쳤다. 2014년 유럽에 램시마가 처음 출시됐을 때만 해도 바이오시밀러에 거부감을 느꼈던 의료진이 적극적으로 돌아섰기 때문이다. 유럽 정부도 가격이 낮으면서 효과가 동등한 바이오시밀러 처방을 적극 장려하고 있다. 그러나 바이오시밀러 개발사가 급증하면서 경쟁이 치열해지고 퍼스트무버 효과가 사라지고 있다는 점은 위협 요인이다.
전예진 기자 ace@hankyung.com