면역치료 효과 없는 암 환자, 이 당단백질이 문제였다
미국 미시간 의대 연구진, 저널 '캔서 셀'에 논문

원래 '면역 관문'(immune checkpoint)은 면역세포 기능을 활성화하면서 면역세포가 자기 세포를 공격하지 않도록 면역 강도를 적절히 조절한다.
그런데 암세포가 면역세포의 공격을 회피하는 데 면역 관문을 이용한다는 게 밝혀져, 역으로 이를 무력화하는 면역 관문 억제 치료가 개발됐다.
하지만 면역 관문 억제제도 중대한 결함을 안고 있다.
약을 쓰는 환자마다 반응의 편차가 너무 크다는 것이다.
실제로 이 치료로 효과를 보는 환자는 일부에 그친다.
면역 관문 억제제의 이런 약점을 보완하는 데 중요한 실마리가 될 수 있는 당단백질(glycoprotein)과 관련 신호 차단 메커니즘을 미국 미시간대 연구진이 발견했다.
스탄니오칼신-1(STC1)으로 불리는 이 단백질이 암 종양이나 면역 기능과 관련해 어떤 역할을 하는지는 거의 알려진 게 없다.
스탄니오칼신은 장(腸)과 신장에서 칼슘, 인 등의 조절에 관여하는 폴리펩타이드(다중 결합 아미노산) 호르몬이다.
미시간 의대 로걸 암센터의 저우 웨이 핑 병리학 면역학 교수팀이 수행한 이 연구 결과는 최근 저널 '캔서 셀'(Cancer Cell)에 논문으로 실렸다.
29일 미국 과학진흥협회(AAAS) 사이트(www.eurekalert.org)에 공개된 논문 개요 등에 따르면 면역계가 T세포를 만들어 암 종양을 공격하려면 암세포의 어떤 신호가 필요한데 이 신호의 전달을 차단하는 게 STC1이다.
이 말은 STC1이 관여하는 경로를 치료 표적으로 삼을 수 있다면 암세포의 '나를 먹어 치워' 신호를 다시 내보낼 수 있다는 뜻이다.
저우 교수와 동료 과학자들은 무슨 역할을 하는지 깜깜했던 STC1이 T세포의 활성도 저하, 흑색종 환자의 낮은 생존율 등과 연관돼 있다는 걸 확인하고 본격적인 연구를 시작했다.
연구팀은 암 유전체 지도(Cancer Genome Atlas)의 데이터베이스를 샅샅이 뒤져, STC1 수위가 높을 때 환자의 생존율이 낮아지는 10개 유형의 암을 추려냈다.
그런 다음 암 종양 내에 SRC1이 있으면 T세포의 항암 반응이 약해진다는 걸 생쥐 실험에서 확인했다.
STC1은 T세포를 자극하는 데 꼭 필요한 항원 제시 세포를 손상했다.
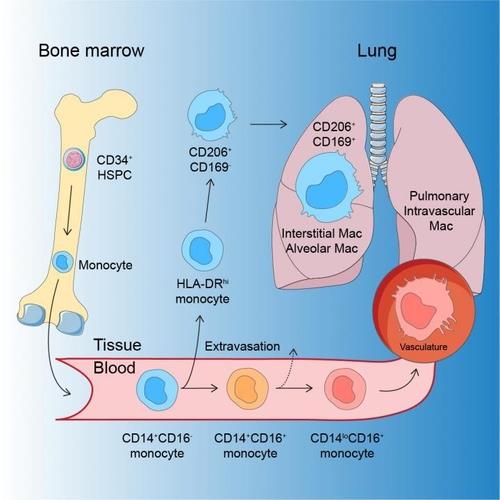
암 종양의 STC1은, 항원 제시 세포이기도 한 대식세포가 죽어가는 암세포를 포식하는 걸 막았다.
대식세포의 암세포 포식은 T세포에 항원을 제시하는 데 꼭 필요한 과정이다.
종양의 STC1이 차단하는 건, 소포체 내강에 존재하는 칼슘 결합 단백질로서 '나를 먹어 치워' 신호의 핵심인 칼레티쿨린(CRT)이었다.
암세포 표면에 CRT가 충분하지 않으면 대식세포가 죽은 암세포를 효과적으로 포식하지 못했다.
이는 곧 차단된 CRT 신호를 풀면 대식세포의 암세포 포식도 원활히 이뤄질 수 있다는 걸 시사한다.
STC1-CRT 상호작용을 조준하는 게 면역 관문 억제 치료의 효과를 배가하는 경로가 될 수 있다는 뜻이기도 하다.
저우 교수는 "T세포 활성화 이전에 회피 전략을 구사하는 암 종양은 T세포에 포착될 수 없다"라면서 "면역치료에 저항하는 암 환자의 종양에선 과도한 STC1이 발현한다"라고 지적했다.
하지만 암세포 안에서 STC1-CRT 경로를 치료 표적으로 하는 건 세포 표면보다 훨씬 더 까다롭다.
보통의 경우처럼 항체가 접근하기 어렵다는 점에서 그렇다.
저우 교수팀은 암세포 안으로 뚫고 들어가 STC1과 CRT의 상호작용을 방해하는 저분자 화합물을 개발하는 데 주력하고 있다.
/연합뉴스
-
기사 스크랩
-
공유
-
프린트













![[오늘의 arte] 독자 리뷰 : 당신의 미술 취향은 무엇인가요](https://timg.hankyung.com/t/560x0/photo/202404/AA.36523699.3.jpg)