식약처, 코로나 '자가검사키트' 국내 첫 허가…"한시적 허용"
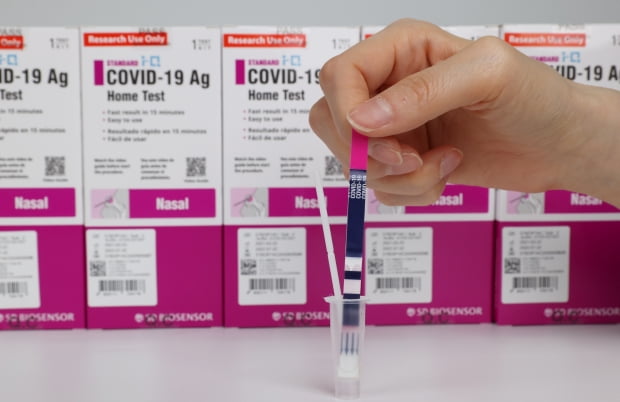
두 진단키트는 각각 에스디바이오센서와 휴마시스 제품이다. 해당 제품은 앞서 국내에서 전문가용으로 허가를 받았고 해외에서는 자가검사용으로 긴급사용승인을 받은 바 있다.
조건부 허가는 정식 허가 제품이 나오기 전에 추가 임상적 성능시험 자료 등을 3개월 이내에 제출하는 조건으로 한시적 사용을 허용하는 제도다.
식약처는 두 제품은 코로나19 확진용이 아닌 보조적 수단으로만 사용해야 한다고 강조했다. 유전자 검사(PCR) 결과와 임상 증상을 고려해 의사가 감염 여부를 최종 판단해야 한다는 의미다.
김수현 한경닷컴 기자 ksoohyun@hankyung.com
-
기사 스크랩
-
공유
-
프린트




!["14억이 전기차 타야하는데"…인도, 리튬·니켈 확보전 뛰어든다 [원자재 포커스]](https://timg.hankyung.com/t/560x0/photo/202404/01.36506152.1.jpg)

![[단독]하이브 키운 '멀티 레이블'이 제 발등 찍었다](https://timg.hankyung.com/t/560x0/photo/202404/02.33877838.1.jpg)