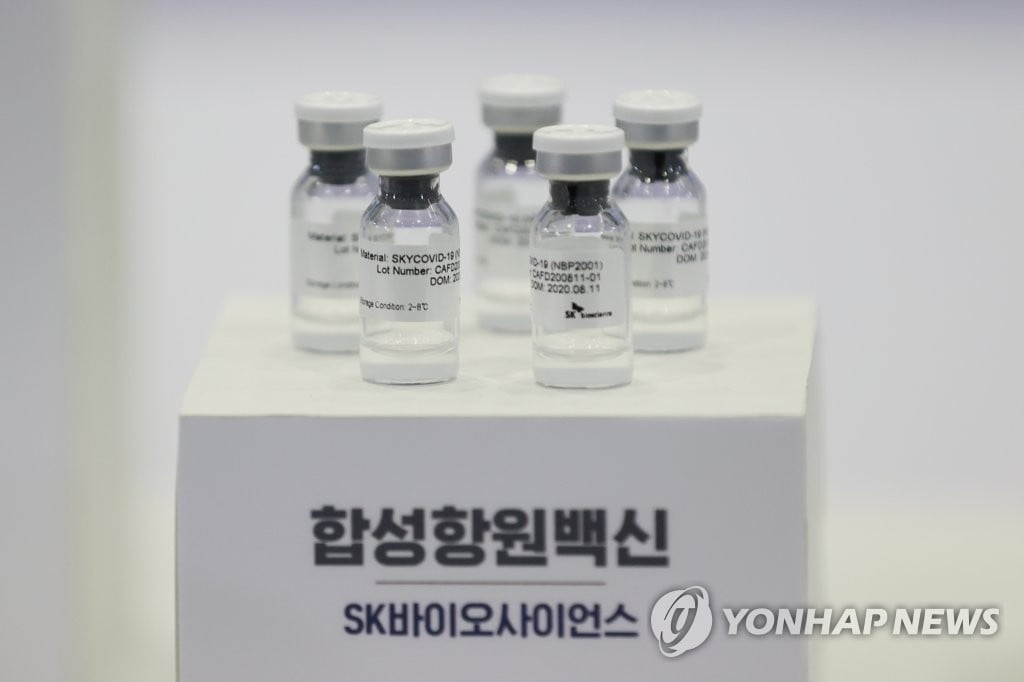
SK바이오 "국내 첫 백신 임상결과 10월에 공개"

김훈 SK바이오사이언스 최고기술책임자(CTO)는 24일 온라인으로 개최된 `2021 제18차 대한백신학회 추계학술대회`에서 회사의 코로나19 백신 후보물질 `GBP510` 향후 개발 계획을 설명하며 이같이 밝혔다.
김 최고기술책임자는 "올해 상반기 임상 1·2상 스터디(시험)에서 우수한 안전성과 효과성을 확인해 이를 기반으로 임상 3상에 돌입했다"며 "회복기 환자 표준혈청보다 5∼6배 높은 중화항체를 보여 선도 백신과 동등한 수준이 아닐까 싶다"고 말했다.
김 최고기술책임자는 그러면서 "자세한 (임상 결과) 자료는 아마도 `CEPI`(전염병대비혁신연합)와 10월 이후 협의를 통해 공개할 수 있을 것 같다"고 덧붙였다. CEPI는 각국 정부와 자선단체 등이 자금을 모아 만든 국제 민간기구로, GBP510의 개발을 지원하고 있다.
김 최고기술책임자는 "국제백신연구소(IVI)와 긴밀히 협력해 임상이 지연되지 않도록 최선을 다하겠다"고 강조했다. SK바이오사이언스는 내년 상반기 내 임상을 끝내고 국내 출시 및 국제 백신 공동구매 프로젝트 `코백스 퍼실리티` 공급 개시를 목표로 하고 있다.
변이 바이러스에 대한 대응 계획에 관한 질문에 김 최고기술책임자는 "델타, 베타 등 변이에 대응하기 위해 `마스터 세포주`까지 만들고 있다"며 "순차적으로 변이 임상에 바로 진입해서 인플루엔자(독감) 바이러스 백신처럼 만들겠다"고 답했다. SK바이오사이언스는 4가 세포배양 독감 백신을 자체 개발한 바 있다.
국내에서 유일하게 코로나19 mRNA 백신 임상시험에 진입한 아이진의 조양제 기술총괄대표도 학회에 참석해 모더나와 화이자 대비 자사 백신 안전성이 우월하다고 강조했다.
조 기술총괄대표는 "PEG(모더나와 화이자 백신 첨가제로 포함된 계면활성제의 일종)에 의한 아나필락시스가 전 세계에서 보고되고 있다"며 "그에 비해 아이진은 PEG를 사용하지 않아서 아나필락시스를 원천적으로 막았다"고 설명했다.
조 기술총괄대표는 "아이진 백신은 주사한 근육 부위에서만 (염증 등) 반응을 유발하고 그 외 심장, 간 등 다른 기관에는 반응을 유발하지 않는다"고 설명했다.
1회 접종용 아데노바이러스 벡터(전달체) 코로나19 백신을 개발하고 있는 셀리드의 강창율 대표는 임상시험 현황과 계획을 구체적으로 공유했다.
셀리드는 임상 2a상을 수행하고 있으며, 백신의 생산성 향상과 생산 원가 절감을 위해 벡터를 변경한 40명 대상 임상 1상도 병행하고 있다.
강 대표는 "다음 주에 임상 1상 대상자 투여를 완료할 예정이며, 내달 중순경에는 진행 중인 모든 스터디(임상시험)가 끝날 것"이라며 "이후 글로벌 임상 2b상과 3상을 계획하고 있으며, 10월 중 국내, 11월 중 베트남과 인도네시아를 포함해 세계보건기구(WHO)에서 임상시험을 허가받을 수 있도록 노력하고 있다"고 말했다.
셀리드는 내년 1분기에 임상시험을 모두 마치고 2분기 허가를 신청하는 것을 목표로 한다.
장진아기자 janga3@wowtv.co.kr
ⓒ 한국경제TV, 무단 전재 및 재배포 금지
-
기사 스크랩
-
공유
-
프린트



![넷플릭스, 가입자 순증 꺾였다…악재 쏟아진 기술주 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202404/B20240419072033320.jpg)


![[단독] "경영보다 돈"…아워홈 매각 손잡은 남매](https://timg.hankyung.com/t/560x0/photo/202404/AA.36472890.1.jpg)





