삼성바이오에피스 "바이오시밀러 유효성·안전성 입증"
삼성바이오에피스는 오는 11일까지 영국 런던에서 개최되는 '2016 유럽 류마티스 학회'에서 바이오시밀러(바이오의약품 복제약) 3개 제품의 임상 결과를 발표했다고 8일 밝혔다.
이번에 발표되는 3개 치료제는 현재 한국과 유럽에서 판매 중인 엔브렐의 바이오시밀러 '브렌시스'(유럽명 베네팔리), 레미케이드의 바이오시밀러 '렌플렉시스'(유럽명 플릭사비)를 비롯해 휴미라의 바이오시밀러 'SB5' 등이다.
회사 측은 "세계 유수의 학회에서 3개 제품의 스위칭 임상 결과를 동시에 발표한 건 삼성바이오에피스가 처음"이라고 소개했다.
스위칭 임상이란 오리지널 약품을 투여받은 환자를 대상으로 일정한 시점에 바이오시밀러로 전환해 임상을 지속하고 유효성, 안전성, 면역원성 등에 차이가 없음을 확인하는 시험을 의미한다.
브렌시스의 임상 3상 결과 브렌시스 지속 투여군과 오리지널 제품에서 브렌시스로 전환한 투여군의 통증 개선도가 각각 77.9%와 79.1%로 유사했다.
브렌시스 임상 3상은 첫 52주 임상을 마친 환자 245명을 대상으로 100주까지 진행됐다.
렌플렉시스의 경우 첫 54주 임상을 끝내고 78주 추가 임상을 진행했다.
연구팀이 ▲ 오리지널 의약품 투약군 ▲ 오리지널 의약품 투약 후 렌플렉시스 전환 ▲ 렌플렉시스 투약군 등 3개 그룹으로 나눠 비교한 결과 세 개 그룹 모두 유효성과 안전성이 모두 유사한 것으로 나타났다.
SB5의 임상 3상 역시 첫 24주를 마친 508명을 3개 그룹으로 나눠 동일한 조건으로 진행한 결과 유효성과 안전성, 면역원성이 모두 유사한 수준이었다.
고한승 삼성바이오에피스 사장은 "이번 임상을 통해 오리지널 제품을 삼성바이오에피스가 개발한 바이오시밀러로 스위칭할 경우 유효성, 안전성 등 모든 측면에서 유사한 수준을 나타낼 수 있다는 사실을 입증했다"며 "앞으로 더 많은 환자에게 의료 혜택의 기회를 부여할 수 있을 것"이라고 말했다.
(서울연합뉴스) 김잔디 기자 jandi@yna.co.kr
-
기사 스크랩
-
공유
-
프린트
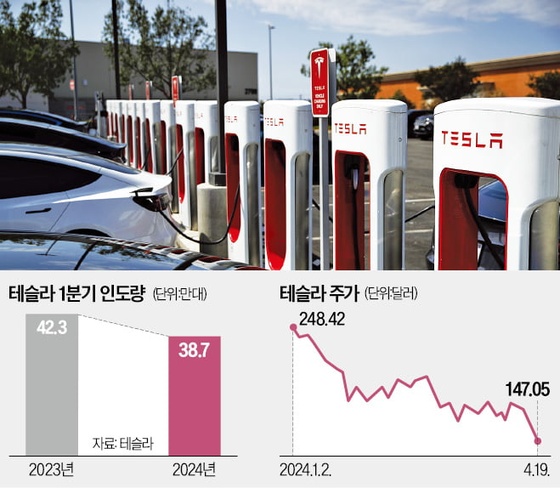
![[속보] 테슬라 1분기 매출 9% 감소, 영업이익 반토막…주가는 반등 왜?](https://img.hankyung.com/photo/202404/02.22579247.3.jpg)

![알약 1000종 AI가 분류한다…메디노드, 시드투자 성공 [Geeks' Briefing]](https://img.hankyung.com/photo/202404/01.36506641.3.jpg)