렘데시비르, 국내 3상서 '부작용' 발견…"심박수 감소" 보고
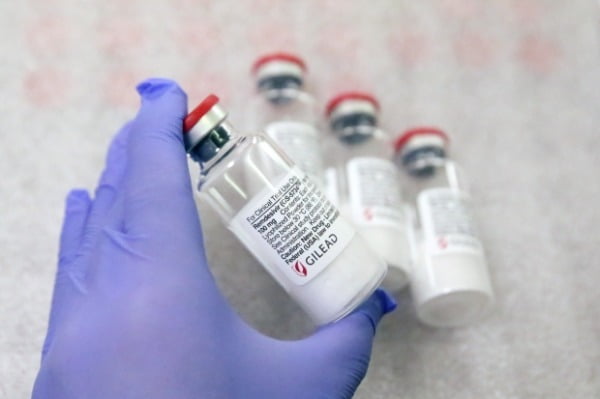
28일 강기윤 보건복지위원회 소속 국민의힘 의원이 식품의약품안전처로부터 받은 자료에 따르면 식약처는 지난 4월 렘데시비르의 '심박수 감소' 부작용을 1건 보고받았다.
해당 부작용은 서울의료원에서 지난 3월27일~6월25일 실시한 3상 임상 단계에서 발생했다.
방역당국에 따르면 지난 7일 기준 국내 환자 274명에게 렘데시비르가 투약됐고, 이 중 16명이 사망한 것으로 알려졌다.
렘데시비르는 길리어드사이언스에서 에볼라 치료제로 개발한 항바이러스제다. 미국 국립보건원(NIH) 주도로 전 세계 10개국, 73개 의료기관에서 시행된 임상시험에서 코로나19 환자의 회복 기간을 15일에서 11일로 약 31% 줄이는 효과를 내 주목을 받았다.
국내 렘데시비르 허가는 조건부 허가다. 조건부 허가는 국제적으로 실시하고 있는 임상시험 최종 결과와 일부 제조 및 품질관리 기준 자료, 추가 위해성 완화조치 등을 시판 후 제출하는 조건으로 이뤄진다. 허가 당시 식약처는 그동안의 전임상시험 문헌 자료와 임상시험 중간 분석 결과를 바탕으로 결정했다고 밝혔다.
이미경 한경닷컴 기자 capital@hankyung.com
-
기사 스크랩
-
공유
-
프린트
![[속보] 서울 19명-경기 14명-경북 4명-부산·인천 등 6곳 각 1명](https://img.hankyung.com/photo/202009/02.22579247.3.jpg)
![[속보] 코로나19 어제 50명 신규확진, 사흘째 두 자릿수](https://img.hankyung.com/photo/202009/ZA.23923373.3.jpg)


!["14억이 전기차 타야하는데"…인도, 리튬·니켈 확보전 뛰어든다 [원자재 포커스]](https://timg.hankyung.com/t/560x0/photo/202404/01.36506152.1.jpg)

![[단독]하이브 키운 '멀티 레이블'이 제 발등 찍었다](https://timg.hankyung.com/t/560x0/photo/202404/02.33877838.1.jpg)



![물가 잡으라는 말에 새벽 4시부터 시장 돌아다닌 공무원들 [서평]](https://timg.hankyung.com/t/560x0/photo/202404/01.36511659.3.jpg)