“파이프라인도 '옥석 가리기'…3상 물질 보유 기업에 주목”
유한양행과 한미약품을 최선호주로, 한올바이오파마와 안트로젠을 관심 종목으로 제시했다.
키움증권에 따르면 지난달 말 기준 미국 상장 바이오텍 451개 중 주요 3상 파이프라인을 보유한 기업의 평균 가치는 8억9700만달러(약 1조2000억원)였다. 이는 코로나19로 바이오 업종이 부각됐던 2021년 말의 7억9700만달러보다 높은 수치다. 반면 전임상 단계 기업의 가치는 2021년보다 85% 급감했다.
이는 금리 상승으로 인해 미래 가치를 당겨와야 하는 전임상 파이프라인에 대한 부담과 성공에 대한 불확실성이 반영되기 때문이라고 봤다.
허혜민 연구원은 “이제는 파이프라인도 옥석을 가리는 시대”라며 “2030년까지 70개 가까운 제품들의 특허만료에 대비하기 위해, 단기에 매출을 창출할 수 있는 후기 단계 파이프라인에 대한 빅파마들의 수요가 커질 것”이라고 말했다.
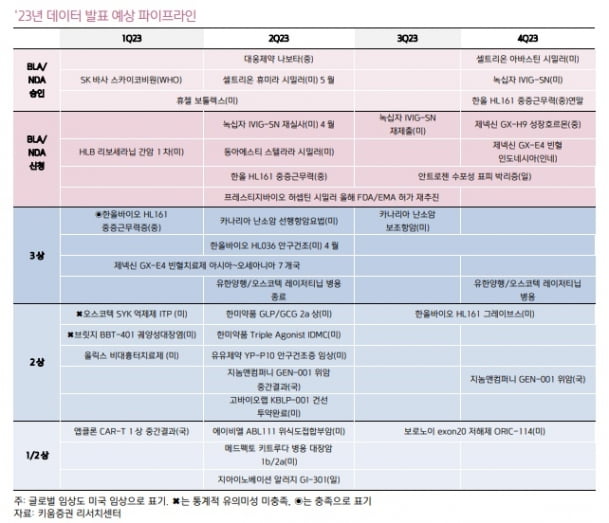
올해 국내 기업들은 후기 단계 파이프라인의 임상 결과(데이터) 발표 및 허가 신청·승인 등 다수의 상승동력(모멘텀)을 보유하고 있다고 했다. 2023년 국산 신약의 해외 승인은 최대 7건, 해외 허가 신청은 9건, 3상 결과 발표는 6건으로 예정돼 있다. 허 연구원은 “허가받으면 가치가 반영될 수 있는 이슈로 대웅제약의 중국 ‘나보타’ 승인과 녹십자의 ‘IVIG-SN’ 미국 승인이 있다”고 했다.
굵직한 3상 발표도 다수 포진돼 있다고 전했다. 한올바이오파마의 ‘HL161’은 최근 중증근무력증 중국 3상에서 유효성을 입증했다. 한올은 안구건조증에서 주 평가지표가 각기 다른 미국 3상과 중국 3상 발표도 앞두고 있다. 유한양행의 ‘레이저티닙’ 병용 3상, 카나리아바이오의 난소암 3상 발표도 예정돼 있다.
안트로젠은 당뇨병성 족부궤양 3상에서 유효성 입증에 실패했지만, 디자인과 제조방법을 변경해 국내 3상과 미국 2상을 진행하고 있다. 국내 3상은 연내 환자 모집을 완료할 예정이다. 결과 발표는 2024~2025년에 다수 예정돼 있다고 했다.
2상 결과 발표를 앞둔 기업도 있다. 오는 2분기에 유유제약의 안구건조증 치료제, 지놈앤컴퍼니와 고바이오랩의 마이크로바이옴 치료제 데이터가 발표될 예정이다. 지난해 말과 올해 초 2상에서 통계적 유의성을 확보하는 데 실패한 펩트론 브릿지바이오테라퓨틱스 오스코텍은 임상 디자인을 변경해 임상 개시 및 기술이전 등을 모색하고 있다.
허 연구원은 “2상은 3상보다 성공 확률이 높지 않지만 성공하면 신약 가치가 재평가되면서 파트너십 협상에 유리한 위치에 선다”고 설명했다.
그는 “삼성바이오에피스는 휴미라 시밀러 ‘하드리마’의 저농도·고농도 제형 모두를 보유하고 있어 안정적인 시장 안착이 예상된다”며 “셀트리온은 아직 휴미라 시밀러의 미국 승인을 받기 전으로, 미국 직접 판매에 성공할 경우 중장기적으로 가격 경쟁에서 유리한 위치를 선점할 것”이라고 말했다.
김예나 기자 yena@hankyung.com
-
기사 스크랩
-
공유
-
프린트












![[오늘의 arte] 독자 리뷰 : 당신의 미술 취향은 무엇인가요](https://timg.hankyung.com/t/560x0/photo/202404/AA.36523699.3.jpg)