“일동제약, 먹는 코로나藥 권리 도입…국내 긴급사용승인 준비”
일동제약은 지난 16일 핑안시오노기와 조코바의 한국 판매권리 및 생산기술 이전에 대한 계약을 맺었다. 조코바는 일동제약이 일본 시오노기제약과 공동 개발 중인 경구용 코로나19 치료제 후보물질이다.
핑안시오노기는 시오노기 홍콩과 중국 핑안보험의 자회사가 2020년 설립한 합작사다. 향후 중국 진출의 거점으로 활용하기 위해 설립했다. 일본을 제외한 아시아 지역의 조코바 개발 및 상업권을 보유하고 있다.
이번 계약으로 일동제약은 핑안시오노기로부터 대한민국 내 상업화 권리 및 생산에 관한 기술 이전받는다. 일동제약이 핑안시오노기에 계약금 450만달러(약 63억원)를 지급하고, 추후 국내 판매에 대한 기술사용료(로열티)를 지불하는 조건이다. 내달까지 국내 긴급사용승인이 완료되면 완제품 뿐 아니라 원료물질 생산에 대한 기술도 이전받게 된다.
조코바의 권리는 일본은 시오노기, 한국은 일동제약, 기타 아시아 지역에선 핑안시오노기가 갖는 것으로 구분됐다. 현재 조코바는 일본 후생노동성에서 긴급사용승인 허가를 진행하고 있다.
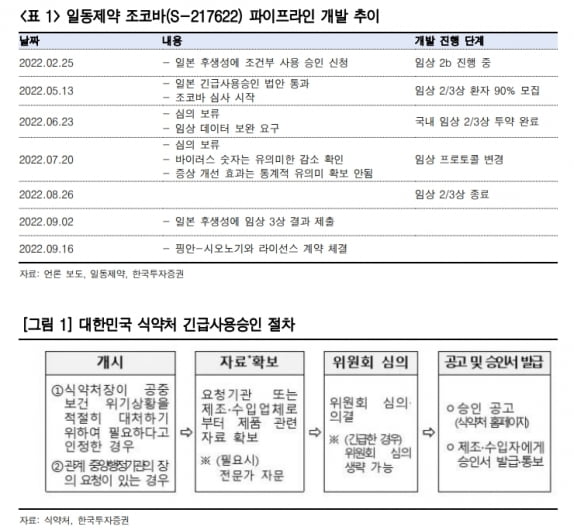
이번 계약은 국내 긴급사용승인을 대비한 사전 준비라는 판단이다. 국내 기업이 생산을 전담하는 경우, 긴급사용승인 과정에서 심사에 소요되는 기간을 단축시킬 수 있다는 것이다.
오의림 연구원은 “한국 식품의약품안전처의 긴급사용승인은 기업이 신청하는 형태가 아닌, 식약처장이 필요성을 인정하거나 관계 중앙행정기관장의 요청이 있는 경우 심사가 진행된다”며 “심의 과정 중에는 제품의 생산 방식, 작용 기전, 효력 및 임상 데이터 등의 자료제출이 요구돼, 국내 기업이 생산을 전담하는 경우 이 과정에서 의사소통이 수월해질 가능성이 높다”고 말했다.
다만 “조코바의 국내 긴급사용승인 여부 혹은 승인 시기를 예상하기는 어렵다”며 “추후 국내 식약처 및 일본 후생성의 발표를 지속적으로 모니터링할 필요가 있다”고 했다.
-
기사 스크랩
-
공유
-
프린트





![하루 만에 550조원 증발…실적·물가 압력에 기술주 투매 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202404/B20240206081554930.jpg)


![[단독] "경영보다 돈"…아워홈 매각 손잡은 남매](https://timg.hankyung.com/t/560x0/photo/202404/AA.36472890.1.jpg)





![[신간] 로마 제국이 '최고 국가'로 우뚝 서기까지…'팍스'](https://timg.hankyung.com/t/560x0/photo/202404/ZK.36477517.3.jpg)