“희귀의약품, K-바이오가 두각 나타낼 분야될 것”
희귀의약품은 낮은 유병률로 인해 치료제를 개발하더라도 수익성이 보장되지 않아 기업들이 관심을 두지 않는 의약품을 말한다. 대표적인 희귀질환으로 비호지킨성림프종(NHL), 급성골수성백혈병(AML), 낭포성섬유증(CF) 등이 있다.
진홍국 연구원은 “과거에는 희귀의약품이 개발에 투입되는 비용에 비해 유병률이 낮아 시장이 제한적이라는 이유로 개발을 소홀히 했다”며 “그러나 최근에는 미국을 포함한 선진국에서 희귀 난치성 질환을 공공보건정책의 우선순위 과제로 두고 있어 향후 연구개발이 기대되는 분야”라고 말했다.
그는 “미국 식품의약국(FDA)은 희귀의약품 개발을 장려하기 위해 개발 업체들에 재정적 인센티브와 다년간의 독점판매권 등을 제공하고, 판매허가 심사도 빠르게 진행하고 있다”며 “개발업체들은 임상 성공률이 높아지고 판매시기도 앞당길 수 있어 유리하다”고 덧붙였다.
희귀의약품 시장은 꾸준히 성장할 것으로 봤다. 시장조사기관 이밸류에이트파마에 따르면 희귀의약품 시장 규모는 2019년 1360억달러에서 2024년 2420억달러로 연평균 12% 성장할 것으로 전망된다. 2024년 전세계 처방의약품 매출 규모가 1조2000억달러라는 점을 감안하면 20% 이상을 희귀의약품이 차지하게 된다는 설명이다.
국내 제약·바이오 산업에서도 투자대안이 될 수 있다고 판단했다. 진 연구원은 “바이오시밀러와 희귀의약품은 경우에 따라 임상 한 단계를 건너뛸 수 있어 비교적 성공 가능성이 높고 출시가 빠르다는 공통점이 있다”며 “희귀의약품이 바이오시밀러 다음으로 국내 업체들이 글로벌 시장에서 두각을 나타낼 수 있는 분야”라고 했다.
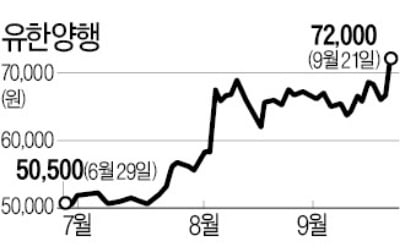
특히 연말 메지온의 신약허가신청(NDA) 승인과 판매허가 획득이 국내 희귀의약품 업체들이 리레이팅하는 주요 이벤트가 될 것으로 예상했다. 메지온은 단심실증 치료제 유데나필에 대해 최근 임상 3상을 마치고 지난 6월 NDA를 제출했다. 문서화 작업 관련 기술적인 이슈로 FDA로부터 보완 요청을 받아 연내 NDA를 다시 제출할 계획이다. 연말 서류 검토가 받아들여진 후 판매허가를 획득한다면 내년 하반기 제품을 출시할 수 있을 전망이다.
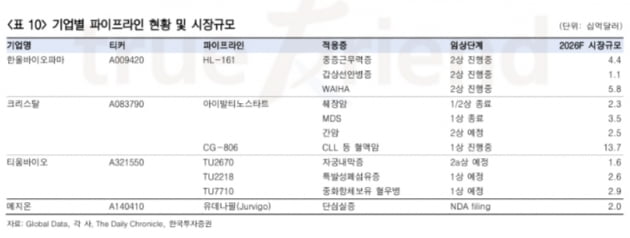
진 연구원은 “희귀의약품 후보물질(파이프라인)이 회사의 핵심 파이프라인이거나, 이미 FDA로부터 희귀의약품 지정(ODD)을 받은 기업에 주목해야 한다”며 “개발하고 있는 적응증의 향후 글로벌 시장규모가 1조원 이상이라면 밸류에이션(실적 대비 주가 수준) 프리미엄 부여도 가능하다”고 했다.
관심종목으로는 한올바이오파마 크리스탈 메지온 티움바이오 등을 제시했다.
-
기사 스크랩
-
공유
-
프린트









!['베니스의 장인들' 르네상스 조선소에 쿵쿵쿵 망치질! 클래스가 달랐던 토즈 전시 [2024 베네치아 비엔날레]](https://timg.hankyung.com/t/560x0/photo/202404/01.36496137.3.jpg)