말기 혈액암 아이 살린 'CAR-T' 국산화 시동
암 인지 수용체 결합한 약물
'기적의 항암제'라 불리기도
앱클론, 구로에 생산시설 준공
큐로셀은 연내 임상 시작 계획
제조 노하우·원료 확보가 관건

앱클론·큐로셀 생산시설 갖춰
CAR-T 치료제는 환자 혈액에서 얻은 면역세포(T세포)와 암을 잘 인지하는 수용체(CAR)를 유전자 조작으로 결합한 뒤 대량 배양한 약물이다. 지금까지 출시된 CAR-T 치료제는 노바티스의 킴리아와 길리어드의 예스카타뿐이다. 킴리아와 예스카타는 지난해 전 세계에서 각각 3000억원, 5500억원어치가 팔렸다. 글로벌 제약사 BMS도 미국에서 CAR-T 치료제 판매허가 절차를 밟고 있다.
국내에선 앱클론과 큐로셀이 CAR-T 치료제 개발 경쟁을 본격화하고 있다. 두 회사는 최근 임상시험에 필요한 시약을 생산할 시설도 갖췄다. 이들이 국내에서 CAR-T 치료제 임상을 처음 시작할 가능성이 높다. 큐로셀은 지난 3월 삼성서울병원에 500㎡ 규모의 CAR-T 치료제 생산시설을 지었다. 앱클론도 지난달 서울 구로동 본사에 같은 규모의 생산시설을 완공했다. 연간 100여 명분의 약물을 생산할 수 있는 규모다.
항체 연구에 주력하던 앱클론은 CAR-T 치료제 전문 기업으로의 변신을 시도 중이다. 지난해 7월 킴리아 개발에 참여한 마르코 루엘라 펜실베이니아 의대 교수를 자문위원으로 영입했다. 경기 시흥에 CAR-T 치료제센터를 구축하기 위해 토지 4276㎡를 87억원에 샀다. 회사 관계자는 “센터 설계 작업을 마쳤다”며 “임상1상을 완료한 뒤 구체적인 착공 일정을 논의할 것”이라고 했다.
큐로셀은 올 3분기 식품의약품안전처에 임상시험계획(IND)을 제출하고 올해 안에 임상을 시작할 예정이다. 이를 위해 삼성서울병원과 협약도 맺었다. 김건수 큐로셀 대표는 “내년 코스닥 상장을 추진하면서 상업화를 위한 공장도 착공할 계획”이라고 했다. 앱클론은 올해 안에 IND를 제출한다는 목표다.
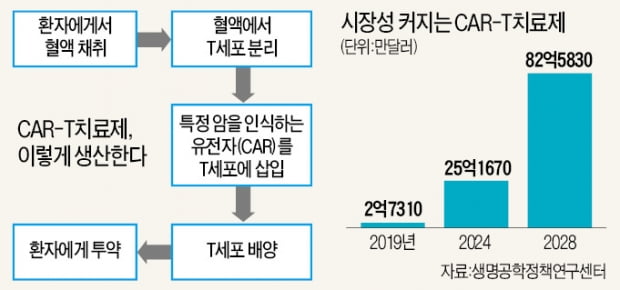
CAR-T 치료제 성공의 열쇠는 제조 노하우다. CAR-T 치료제는 개인 맞춤형 치료제이기 때문에 대량 생산이 원천적으로 어렵다. 앱클론 관계자는 “세포를 배양하는 데 어떤 배양액을 어느 농도로 사용할지는 회사마다 차이가 있다”며 “CAR-T세포를 배양하는 공정을 효율화하고 이를 표준화하는 일이 비교우위를 결정한다”고 했다. 노바티스와 길리어드는 수작업과 장비를 배합해 공정을 개발했다. 앱클론은 전자동 세포배양기를 이용한다. 수작업으로 인한 오염 위험을 줄일 수 있다는 이유에서다. 큐로셀은 면역세포가 암세포를 공격하는 것을 방해하는 단백질인 TIGIT를 없애는 방식으로 효능을 높였다. 실험실 연구 결과 킴리아에 비해 효능이 두세 배 좋다는 게 회사 측 설명이다.
개발 전략을 잘 세우는 것도 중요하다. 예스카타는 킴리아보다 뒤늦게 출시됐지만 매출은 더 높다. 환자 수가 더 많은 적응증으로 허가받았기 때문이다. T세포에 CAR를 결합하는 데 사용되는 바이러스 원료를 원활히 확보하는 것도 과제다. 세계적으로 바이러스 생산 시설이 부족해 공급이 수요를 따라가지 못하고 있어서다. 바이러스는 1회분이 4000만원 이상일 정도로 비싸다. 바이러스를 외부에서 공급받던 기업들이 최근 자체 생산하는 쪽으로 움직이는 이유다.
임유 기자 freeu@hankyung.com
-
기사 스크랩
-
공유
-
프린트











![[오늘의 arte] 독자 리뷰 : 당신의 미술 취향은 무엇인가요](https://timg.hankyung.com/t/560x0/photo/202404/AA.36523699.3.jpg)