"운동선수나 젊은이 급성 심장사, 원인은 심장 과로"
하버드의대 연구진, 미 심장협회 회보 '순환계'에 논문
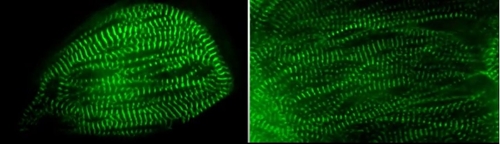
HCM은 건강해 보였던 젊은이나 운동선수한테 갑자기 발생하는 급성 심장사의 주요 원인으로 꼽힌다.
소아 환자의 50~60%에 가족력이 있어 일종의 유전 질환으로 여겨지기도 한다.
그런데 심장의 수축성 단백질인 미오신(myosin) 제어 유전자의 결함이 HCM의 원인이라는 걸 미국 하버드대 의대 과학자들이 발견했다.
이 유전자의 돌연변이로 활성 미오신과 비활성 미오신의 균형이 깨지면, 심장의 정상적인 수축·이완 기능이 교란돼 HCM을 유발한다는 것이다.
하버드 의대 블라바트닉 연구소의 크리스틴 세이드먼 유전학 교수팀은 27일(현지시간) 미국 심장협회 회보 '순환계(Circulation)'에 관련 논문을 발표했다.
온라인(www.eurekalert.org)에 공개된 논문 개요 등에 따르면 이 발견은, 심장 근육 기능에 핵심적 작용을 하는 진화적 메커니즘을 처음 밝혀냈다는 점에서 우선 주목된다.
후속 연구를 거쳐 검증이 이뤄지면, 부정맥이나 심부전같이 흔히 발생하는 심장질환의 진행을 막고, 예방을 돕는 치료법 개발로 이어질 수 있다는 것이다.
현재 HCM 치료는, 증상을 완화하는 약물을 투여하거나, 두꺼워진 심근을 외과 수술로 절제하거나, 심방세동기(cardioverter defibrillators)를 이식하는 정도에 그친다.
평생 심장이 정상적으로 뛰는 건, 심장 근육 세포에 있는 미오신 단백질이 '분자 모터(molecular motor'처럼 온·오프를 반복하면서 심근의 수축과 이완을 제어하기 때문이다.
미오신은 다른 단백질과의 교차 결합을 통해 근육 세포가 수축하게 한다.
그런데 미오신 단백질이 과도히 활성화하면 심장 근육이 지나치게 수축하면서 이완 작용이 정상적으로 이뤄지지 않는다는 게 이번에 입증됐다.
이런 식으로 심장의 과로가 지속하면 결국 심근이 두꺼워지는 HCM이나 심부전 등으로 이어진다는 것이다.
이전의 생쥐 실험에선 심장이 정상일 때 미오신의 온·오프 비율이 약 '2 대 3'으로 보고됐다.
또한 동면 중인 다람쥐의 경우 심장 박동이 약 1분에 6회로 줄고, 비활성 미오신은 정상 다람쥐(분당 심박 수 340회)보다 10%가량 많다는 것도 확인됐다.
하지만 심장 근육 세포에 HCM 돌연변이가 생기면 과다한 미오신이 동작 준비 상태에 들어가 적정 비율이 무너진다는 게 새롭게 밝혀졌다.
이같이 미오신의 활성도를 조절해 심장 근육의 수축을 제어하는 메커니즘은 종(種) 전반에 걸쳐 진화적으로 보전된 것으로 확인됐다.
세이드먼 교수팀은 이미 외부 생명공학 회사에서 개발한 저분자 약물을 인간과 생쥐의 심장 세포에 투여해, 심장의 근육 수축과 에너지 소비가 정상으로 돌아오는 걸 확인했다.
이 회사는 논문의 저자들이 공동 설립한 것이며, 이 약물은 현재 임상 시험 과정에 있다고 연구팀은 전했다.
논문의 수석저자인 세이드먼 교수는 "대사 스트레스를 받아 많은 에너지를 쓰는 만성 과로 상태의 심장 세포가 어떻게 HCM을 일으키고 결국 부정맥이나 심부전으로 이어지는지를 이젠 설명할 수 있게 됐다"라고 말했다.
/연합뉴스
-
기사 스크랩
-
공유
-
프린트

![[포토] 분열된 美대학…親이스라엘·親팔레스타인 시위대 격돌](https://img.hankyung.com/photo/202404/AA.36504166.3.jpg)