화이자, 英 항바이러스업체 6400억원에 인수[이우상의 글로벌워치]

RSV는 급성호흡기감염병을 일으키는 바이러스다. 국내에서도 늦가을부터 겨울철까지 유행하는 대표적인 호흡기 바이러스다. 유아나 노인 등 고위험군이 감염될 경우 폐렴으로 이어져 치명적일 수 있다. 세계적으로 매년 6400만명이 감염되고 16만명이 사망하는 것으로 알려졌으나, RSV에 대한 치료제나 백신은 아직 개발되지 않았다.
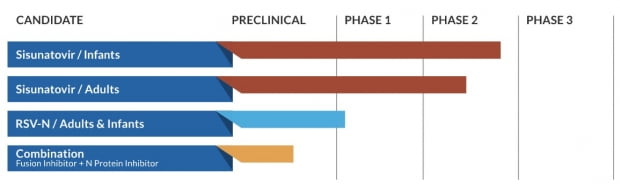
화이자는 이번 인수를 통해 리바이럴이 보유한 다수의 RSV 항바이러스제 후보물질(파이프라인)을 확보했다. 미국 식품의약국(FDA)으로부터 신속심사(패스트트랙) 지정을 받은 시수나토비르(Sisunatovir)의 개발 진도가 가장 빠르다. 시수나토비르는 RSV가 숙주 세포와 융합하는 것을 억제하는 경구용 치료제다.
건강한 성인 200명을 대상으로 한 임상 2상에서 체내 바이러스량(viral load)을 유의미하게 감소시키는 결과를 냈다. 시수나토비르는 RSV에 대한 대표적인 취약군인 유아 184명을 대상으로 임상 2상을 진행하고 있다. RSV의 복제를 막는 또 다른 항바이러스제 후보물질(RSV-N)은 임상 1상 단계에 있다. 시수나토비르와 RSV-N을 병합한 병용요법은 전임상을 진행 중이다.
RSV는 특화된 치료방법이 없는 반면, 영유아를 중심으로 세계적으로 감염 사례가 많아 글로벌 제약사들이 백신 및 치료제 개발을 위해 눈독을 들이는 병원체다. 예방 목적의 항체로는 사노피와 아스트라제네카가 공동 개발한 니르세비맙(Nirsevimab)이 가장 허가에 임박한 것으로 평가받고 있다. 유아 1490명을 대상으로 한 임상 3상(MELODY)에서 니르세비맙은 위약 대비 폐렴 등 호흡기 감염증 발생률을 위약 대비 74.5% 낮췄다. 아스트라제네카는 당국에 허가신청을 준비하고 있다.
미국 머크(MSD)는 모더나와 공동개발 중이던 백신 후보물질(mRNA-1172)에 대한 권한을 2020년 반환하고 독자 개발에 나섰다. MSD가 자체 개발한 RSV 백신 후보물질 ‘MK-1654’는 지난해 11월 임상 3상을 시작했다. 1세 이상 유아 1000명이 대상이며 MK-1654와 위약 외에도 RSV가 유발하는 중증 하기도감염을 예방하는 팔리비주맙(palivizumab)까지 비교하는 임상시험이다.
이우상 기자
-
기사 스크랩
-
공유
-
프린트
![美 선샤인바이오, 주가 178% 폭등…mRNA 항암제 결과 발표[이우상의 글로벌워치]](https://img.hankyung.com/photo/202204/01.29551377.3.jpg)



![하루 만에 550조원 증발…실적·물가 압력에 기술주 투매 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202404/B20240206081554930.jpg)


![[단독] "경영보다 돈"…아워홈 매각 손잡은 남매](https://timg.hankyung.com/t/560x0/photo/202404/AA.36472890.1.jpg)





![[신간] 로마 제국이 '최고 국가'로 우뚝 서기까지…'팍스'](https://timg.hankyung.com/t/560x0/photo/202404/ZK.36477517.3.jpg)