툴젠, mRNA 기반 혈우병 치료제 연구성과 국제학술지 게재
유전자가위 mRNA를 지질나노입자로 전달
이번 연구는 염수청 서울대 교수팀, 이혁진 이화여대 교수팀과의 공동연구로 진행됐다. A·B형 혈우병 생쥐에게 mRNA 기반 약물을 체내로 전달해 치료 가능성을 확인하는 데 성공했다는 설명이다.
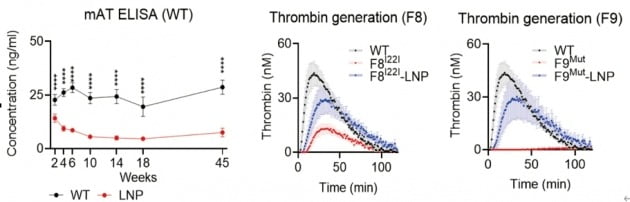
연구팀은 간에서 발현하는 ‘안티트롬빈’ 유전자를 저해하는 유전자교정 치료제 개발을 연구했다. 기존 응고인자 단백질에 대한 항체가 생겨 치료가 어려운 환자를 포함, 거의 모든 혈우병 환자들이 치료대상이 될 수 있다는 설명이다.
혈우병은 피가 멎지 않는 질환이다. 혈액응고인자의 돌연변이로 발생한다. 현재 사용 중인 응고 단백질 치료제는 반감기가 짧아 며칠 또는 몇 주에 한 번씩 평생 투여해야 한다. 또 부족한 응고인자를 단백질 치료로 보충받을 경우, 응고인자에 대해 항체가 생겨 치료 효과가 줄어드는 경우가 많다.
연구팀은 부족한 응고인자를 직접 채워주는 기존 방식과 달리, 안티트롬빈 유전자를 조절해 혈액 응고에 필수적인 효소인 ‘트롬빈’의 형성을 촉진시켰다. 안티트롬빈 유전자를 교정하는 유전자가위를 만드는 mRNA를 지질나노입자(LNP)로 전달했다. 이를 통해 혈중 안티트롬빈 양을 70% 이상 감소시키고, 효과가 10개월 이상 지속되는 것을 확인했다.
특히 수일 내에 체내에서 대사될 수 있는 LNP를 사용해, 필요한 시간 동안만 유전자교정 도구를 세포에 노출시키는 안전한 방법을 사용했다는 설명이다.
이혁진 교수는 “이번 연구에 사용된 이온화 LNP는 기존 양이온 LNP의 낮은 전달효율과 독성을 극복할 수 있도록 자체 개발됐다”며 “크리스퍼는 원하는 교정을 위한 시간이 많이 필요하지 않아 생체 내에서 반감기가 짧은 LNP가 바이러스 전달체보다는 안정성 확보 측면에서 더 적합할 수 있다”고 말했다.
김영호 툴젠 대표는 “혈우병은 유전질환 중에서도 환자가 많아, 10조원 이상의 큰 시장을 형성하고 있다”며 “앞으로 진행할 비임상 시험 등을 빠르게 마쳐 임상에 진입, 차별화된 기전으로 기존 제품들과 경쟁할 수 있도록 노력하겠다”라고 했다.
이도희 기자
-
기사 스크랩
-
공유
-
프린트




!['매그니피센트7' 실적 먹구름…지수 혼조 [뉴욕증시 브리핑]](https://timg.hankyung.com/t/560x0/photo/202404/01.36519299.1.jpg)







![살인과 고문조차 서슴치 않았던 폐륜의 과학자와 의사들 [서평]](https://timg.hankyung.com/t/560x0/photo/202404/01.36520524.3.jpg)