식약처 검증자문단 "모더나 코로나 백신, 허가 가능한 수준"
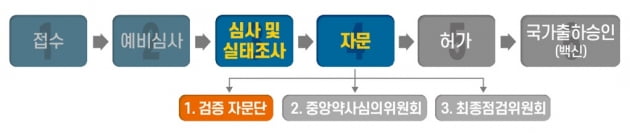
검증 자문단은 중앙약사심의위원회 자문에 앞서 식약처가 임상 비임상 품질 등 다양한 분야의 전문가들에게 자문 의견을 수렴하는 절차다. 전날 열린 검증 자문단 회의에는 감염내과 전문의, 백신 전문가 및 임상 통계 전문가 등 7명이 참석했다.
자문단은 모더나 코로나19 백신의 안전성과 효과성에 대해 주로 미국에서 수행된 임상 3상 자료를 통해 평가했다.
모더나 백신 2차 투여 14일 이후 코로나19로 확진받은 사람은 백신군 11명, 대조군 185명으로 약 94.1%의 예방효과가 나타났다. 연령과 기저질환 유무에 관계없이 86% 이상의 예방효과가 있었다. 자문단은 18세 이상 2차 투여 14일 후 효과가 확인돼, 허가를 위한 예방 효과는 인정 가능하다고 판단했다.
안전성에 있어서도 임상시험에서 발생한 이상 사례와 관련해 허용할 만한 수준이라고 봤다. 또 허가 후 안전성 확보를 위해 '위해성관리계획'을 통해 임상시험 중 나타난 이상사례 등을 추가로 관찰하고 정보를 수집해 평가하는 것이 타당하다는 의견을 전했다.
식약처는 오는 13일 식약처의 법정 자문기구인 중앙약사심의위원회에서 신청 품목의 안전성, 효과성, 허가 시 고려해야 할 사항 등에 대해 2차 자문을 받는다. 결과는 당일 오후에 공개할 계획이다.
한민수 기자
-
기사 스크랩
-
공유
-
프린트

![하루 만에 550조원 증발…실적·물가 압력에 기술주 투매 [글로벌마켓 A/S]](https://timg.hankyung.com/t/560x0/photo/202404/B20240206081554930.jpg)


![[단독] "경영보다 돈"…아워홈 매각 손잡은 남매](https://timg.hankyung.com/t/560x0/photo/202404/AA.36472890.1.jpg)





