바이오엔테크 CEO "코로나19 백신 12월 공급 가능성" 재언급
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
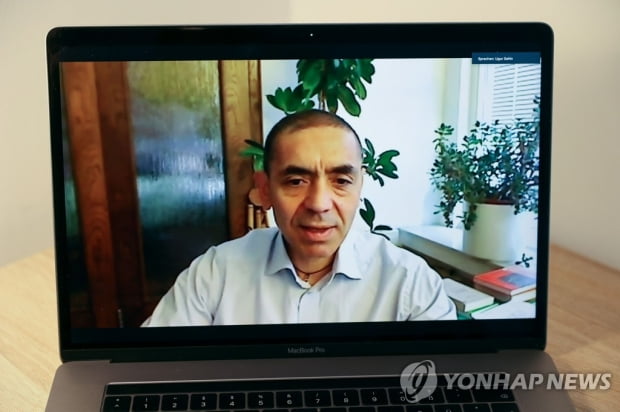
우구어 자힌 바이오엔테크 CEO는 19일(현지시간) AFP 통신과의 인터뷰에서 미국 화이자와 함께 개발 중인 코로나19 백신이 "올해 안으로 미국과 유럽지역에서 사용 승인을 받을 가능성이 있다"고 말했다.
자힌 CEO는 "우리는 전속력으로 일하고 있다"면서 "모두 매우 긴밀하게 협력한다면 우리는 12월에 백신을 유통하기 시작할지 모른다"고 강조했다.
그는 백신의 긴급사용을 위한 서류를 오는 20일 미국 식품의약국(FDA)에 제출할 것이라고 확인했다.
자힌 CEO는 전날 CNN방송, 로이터TV와의 인터뷰에서도 이런 입장을 밝힌 바 있다.
긴급사용 승인은 공중보건 위기 시 의약품의 활용도를 높이기 위한 일시적 조치다.
정식사용 승인 절차보다 승인 요건이 상대적으로 엄격하지 않다.
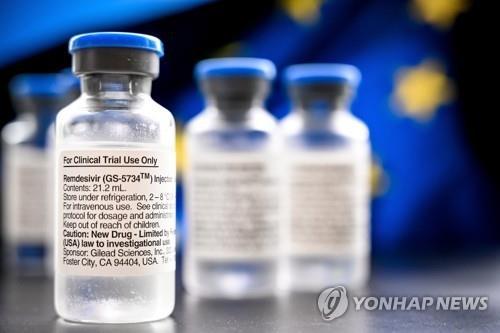
앞서 화이자는 전날 3상 임상시험 단계에 있는 자사 백신에 대한 최종 분석 결과 감염 예방효과가 95%에 달한다고 발표했다.
이는 종전 발표치인 90%보다 크게 상향조정된 것이다.
/연합뉴스


![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


