中 규제개혁 가속페달…한국은 임상 경쟁력↓
한국 7위…"지원책 서둘러야"
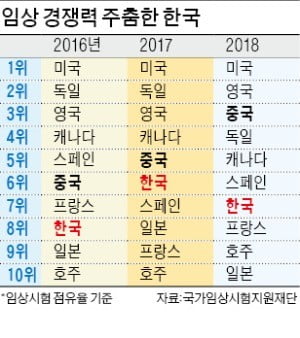
중국은 2017년부터 자국 내 신약 개발을 지원하기 위해 대대적으로 규제 개혁에 나섰다. 60일 안에 임상시험 승인 여부를 결정하는 것은 물론 임상 인력 확충, 승인 절차 간소화, 우선심사제도 확대, 임상시험 실시기관 기준 완화, 해외 임상데이터 인정 등 대대적으로 임상시험 제도를 손질했다. 그 덕분에 지난해 중국의 임상시험 건수는 전년 대비 34.4% 늘었다.
호주도 임상시험 최적지로 떠오르고 있는 나라다. 호주는 임상시험 승인통지제도를 시행하고 있다. 기업이 임상시험 계획을 규제기관에 제출한 뒤 문제점이 발견되지 않고 일정 기간이 지난 후 기관의 답변이 없으면 자동으로 승인된다. 임상시험 비용에 매기는 세금의 43.5%도 환급해준다. 호주에서 시행한 임상 결과는 신뢰도가 높아 미국, 유럽 등에서 쉽게 수용된다.
스페인과 네덜란드는 올해부터 유럽연합(EU) 전역에서 새로 시행되는 ‘임상시험 EU 공동 승인제도’를 선제적으로 도입했다. 유럽식품의약청(EMA)으로부터 임상시험 승인을 받으면 모든 EU 회원국에서 임상을 시작할 수 있다. 임상시험 계획서를 EU 회원국이 열람할 수 있는 플랫폼인 ‘VHP-PLUS’도 운영 중이다.
임유 기자 freeu@hankyung.com
-
기사 스크랩
-
공유
-
프린트











![[오늘의 arte] 독자 리뷰 : 당신의 미술 취향은 무엇인가요](https://timg.hankyung.com/t/560x0/photo/202404/AA.36523699.3.jpg)